研究 (Research)
最終更新日:
炭素を埋め込み輪をつくる新しいカップリング反応の実現 (Catalytic vinylene transfer reaction for the direct construction of multi-ring systems)
講師 西井 祐二(工学研究科 応用化学専攻) NISHII Yuuji(Graduate School of Engineering)
研究の概要
有機分子中に含まれる炭素–水素結合を金属触媒によって切断し、2炭素ユニットを組み込み新たな環構造を組み上げる斬新なカップリング反応(ビニレントランスファー法)を開発した。安価な固体試薬である炭酸ビニレンが、アセチレンガスの合成等価体として機能することを世界で初めて実証し、炭酸(水+二酸化炭素)のみを副生するクリーンな化学変換を実現した。本反応の開発によって、機能性材料の基礎骨格として広く用いられている、様々な縮環芳香族化合物を迅速に構築することが可能となった。
研究の背景と結果
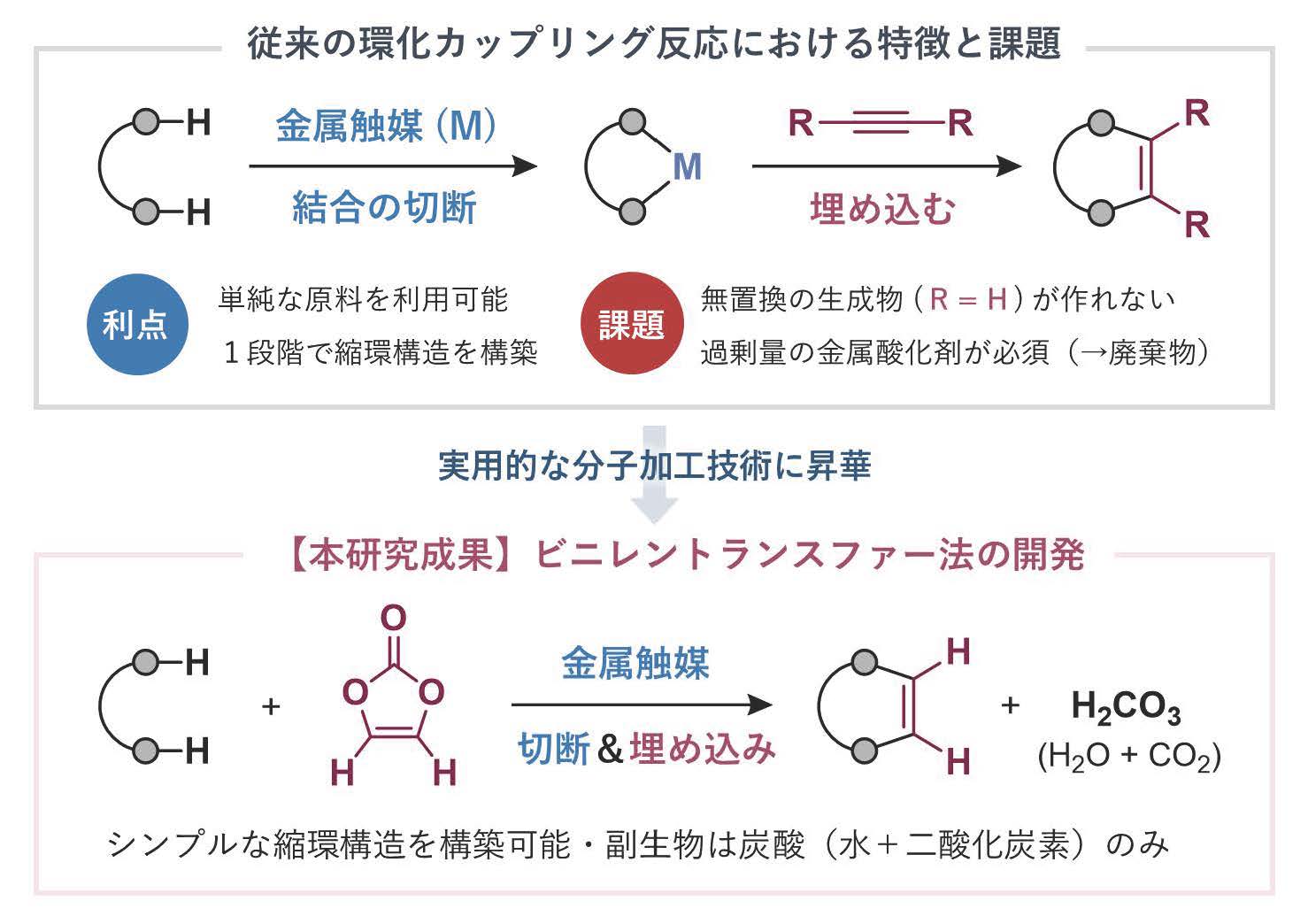
有機合成化学は世界最小の「ものづくり」に挑む研究分野であり、基本単位となる炭素-炭素結合を効率的に組み上げる新たな方法論の確立は、重要なミッションとして認識されている。最近では、有機分子中に普遍的に含まれる炭素–水素結合を、金属触媒を利用して切断する「C-H活性化」と呼ばれる反応が注目を集めている。特に、インドールなどに代表される多環芳香族化合物は「機能の宝庫」と呼べるほど多種多様な化学製品に利用されており、その基礎骨格を1工程で構築する環化カップリング反応は、革新的な手法として脚光を浴びるはずだった。しかし実際のところ、下記2つの問題点のため実用性に欠ける技術となっている。まず1点目に、この反応では置換基を持たない環構造 (R = H) を構築することができず、本来必要としない余分な置換基が生成物に残ることは、特定のターゲット分子の合成を実現するための障害となる。2点目として、カップリング反応の触媒サイクルを成立させるためには、当量以上の酸化剤が必要となる。多くの場合、酢酸銅(II)や酢酸銀(I)などの金属塩が酸化剤として使用されるため、1分子の目的化合物を得るためには、それ以上の量の金属廃棄物が副生してしまう。
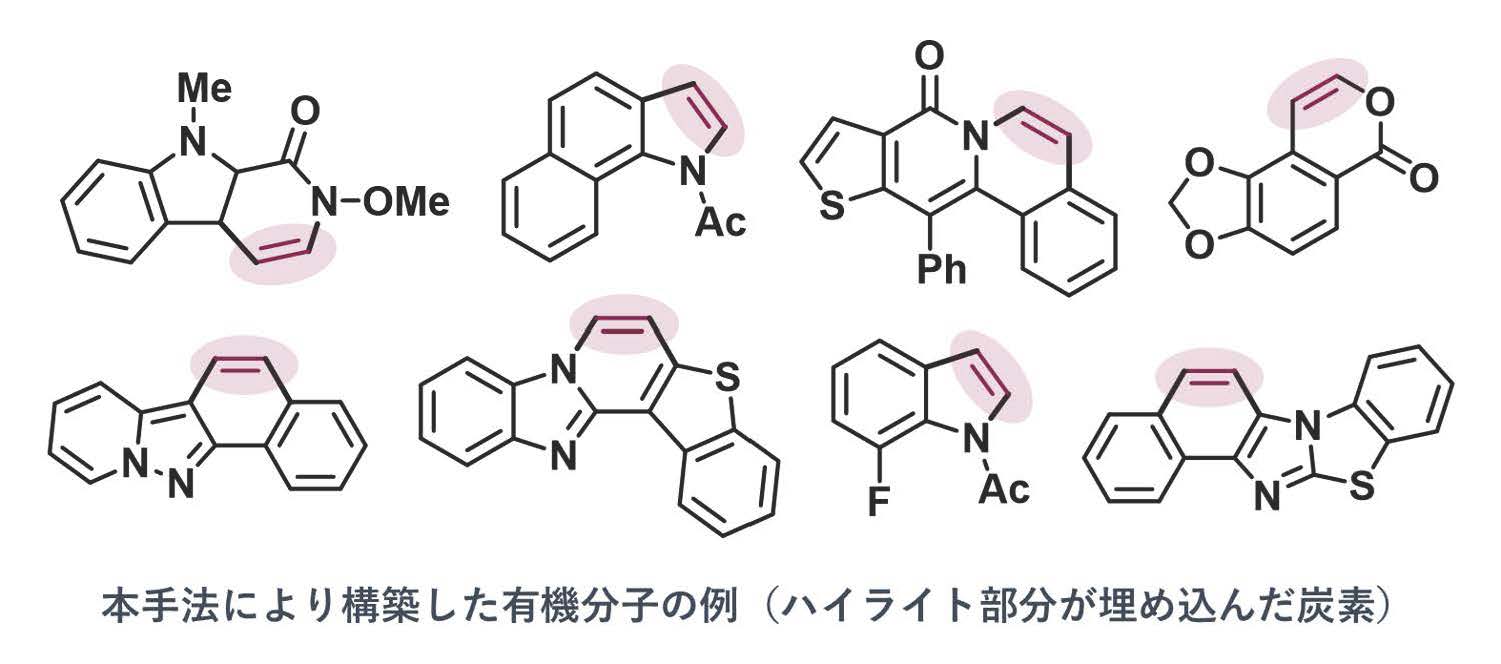
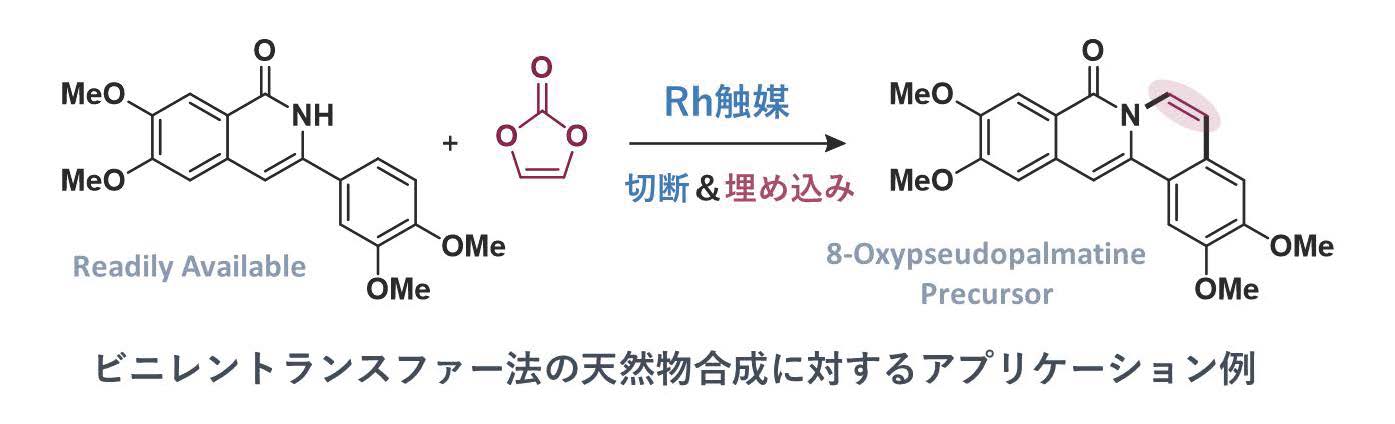
私達の研究グループでは、上記の課題点を解決することができれば、実用性の高い強力な合成ツールに昇華できると考え、炭酸ビニレンを利用したビニレントランスファー法を開発した。炭酸ビニレンは安定な固体の化合物であり、電解液やポリマー原料として安価に入手できるが、この試薬がアセチレンガスの合成等価体として機能することを世界で初めて実証した。本手法では、カップリング反応における副生成物は炭酸(二酸化炭素+水)のみとなり、極めてクリーニングな反応システムが構築できた。ビニレントランスファー法の開発によって、形式的なアセチレン環化反応が簡便に実施可能となり、様々な多環芳香族分子化合物の迅速構築が可能となった。
研究の意義と将来展望
「置換基を持たない」多環構造は、有機合成分野におけるターゲット構造として良く見られるものではあり、本研究で開発したビニレントランスファー法は、その最もシンプルかつ革新的な構築手法を提供するものである。多環芳香族化合物は「機能の宝庫」と呼べるほど様々な機能性材料に利用されており、特に、有機ELや薄膜太陽電池などの有機エレクトロニクス分野に高い利用価値があると考える。また「環化カップリング反応でしか構築できない」分子骨格が多数あることを踏まえると、今まで見過ごされてきた分子の価値を再発見することで、創薬・超分子化学・マテリアルサイエンスなど関連分野に波及効果が期待できる。
担当研究者
講師 西井 祐二(工学研究科 応用化学専攻)
キーワード
触媒化学/有機エレクトロニクス/カップリング反応
応用分野
有機半導体/有機EL/創薬化学
