研究 (Research)
最終更新日:
Resiquimod内封リポソームを使用した腫瘍随伴マクロファージの再教育による抗体依存性細胞貪食の増強 (Enhancing antibody-dependent cellular phagocytosis by re-education of tumor-associated macrophages with resiquimod-encapsulated liposomes)
准教授 曽宮 正晴、教授 黒田 俊一(産業科学研究所 生体分子反応科学研究分野) SOMIYA Masaharu , KURODA Shun'ichi(SANKEN (The Institute of Scientific and Industrial Research))
研究の概要
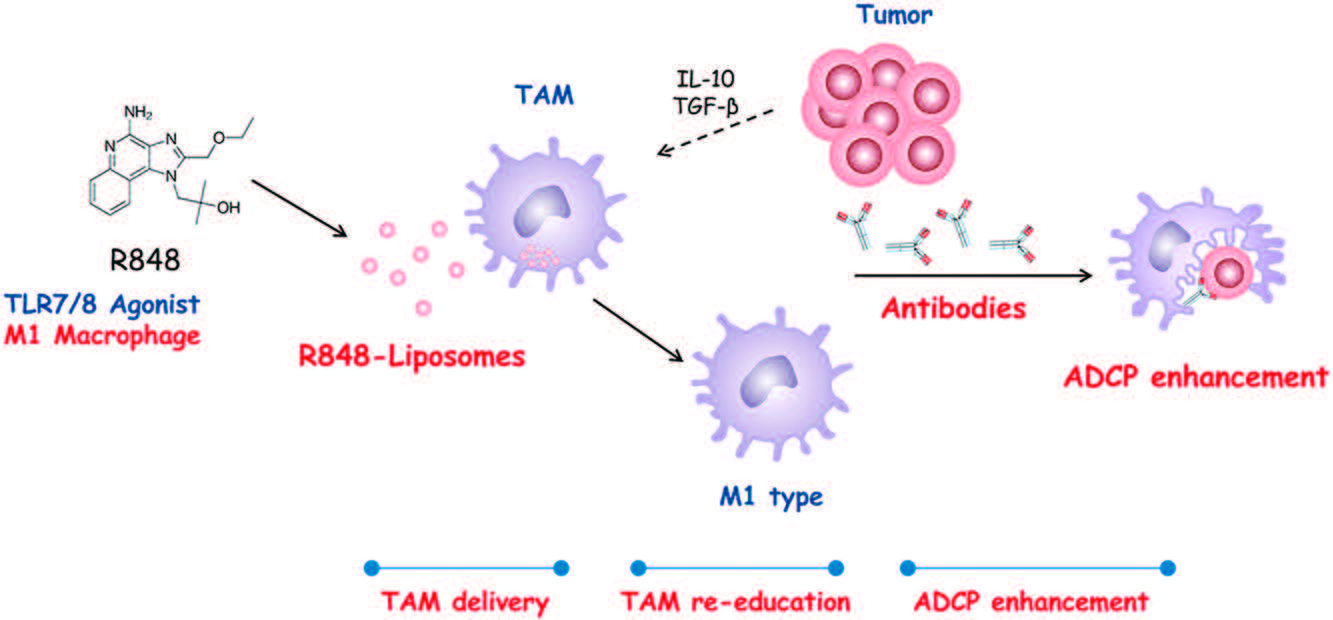
本研究ではマウス腫瘍移植モデルにおいて、腫瘍組織に存在するマクロファージ(tumor-associated macrophage, TAM)にTLR7/8アンタゴニストであるresiquimod(R848)をリポソームによって送達することで、TAMの表現系を腫瘍促進的なM2タイプから抗腫瘍的なM1タイプに再教育し、抗体医薬品の効果を増強させることに成功した。In vitroおよびin vivoの解析の結果より、R848リポソームがマクロファージをM2からM1タイプに変換し、抗体依存性細胞貪食(antibody-dependent cellular phagocytosis, ADCP)の活性を増強して、マクロファージによる腫瘍細胞の貪食を促進することが判明した。またR848内封リポソームは、腫瘍移植マウスに静脈内投与すると腫瘍組織へ蓄積し、TAMに効率的に取り込まれることがわかった。腫瘍移植マウスにR848内封リポソームを投与後、腫瘍を標的とする抗体を投与することで、腫瘍の増殖を顕著に抑制できることを示した。
研究の背景と結果
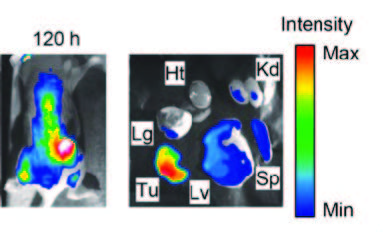
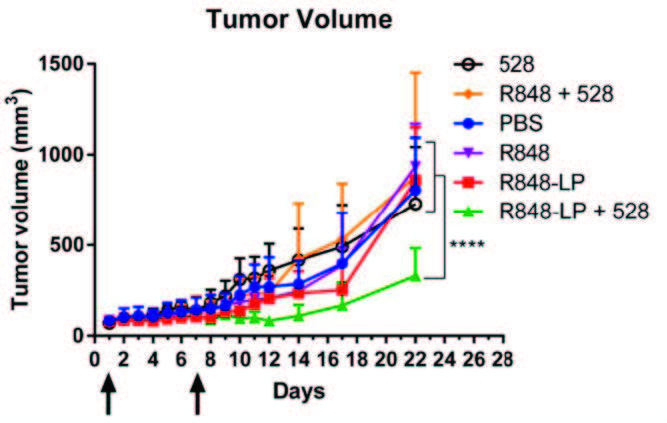
マクロファージは、がん組織において腫瘍の成長、抗腫瘍免疫の抑制、転移などにも関与している、重要な治療標的である。特に腫瘍組織に存在するマクロファージは、腫瘍随伴マクロファージ (tumor-associatedmacrophage, TAM) と呼ばれており、腫瘍の増殖を助ける M2タイプの TAM が多く、この M2-TAM を抗腫瘍的な M1タイプに再教育することで、がん治療の効果を向上させることができると期待されている。特にマクロファージは、抗体を介してがん細胞を貪食する抗体依存性細胞貪食(antibody-dependent cellular phagocytosis, ADCP) によって抗腫瘍効果を発揮することが知られており、TAMのM1タイプへの誘導は、ADCPによって抗体医薬品の効果を増強させることができると考えられる。本研究では、まずM2とM1のマクロファージのADCP活性を比較し、M1タイプのマクロファージが顕著に高いADCP活性を示すことを明らかにした。次に、R848処理によってM2タイプからM1タイプへマクロファージの表現系を変換して再教育できることを示した。さらにR848を内封したリポソームでも、R848単独と同様にマクロファージの再教育及びADCP活性の増強が確認できた。R 848リポソームを腫瘍移植マウスに静脈内投与すると、腫瘍組織に蓄積することがわかり、さらに腫瘍組織内のマクロファージに主に取り込まれていることを確認した。R848内封リポソームおよび抗EGFR抗体を投与した腫瘍移植マウスでは、対照群のマウスと比較して顕著に腫瘍の増殖が抑制された。この抗腫瘍活性は、腫瘍組織中のマクロファージがM2からM1に再教育されていることに由来するものであることが示唆された。
研究の意義と将来展望
R848内封リポソームを投与することで腫瘍組織内のTAMをM2からM1タイプへ再教育し、ADCPを介して抗体医薬品の効果を増強できることを示した。これは従来使用されている抗体医薬品の抗腫瘍効果をさらに増強させる新たな治療戦略の確立につながると期待できる。
担当研究者
准教授 曽宮 正晴、教授 黒田 俊一(産業科学研究所 生体分子反応科学研究分野)
キーワード
リポソーム/DDS/マクロファージ/TLRアンタゴニスト/抗体医薬
応用分野
医療・ヘルスケア/創薬
