研究 (Research)
最終更新日:
インフルエンザに合併する細菌性肺炎の重症化機構の解明 ~新規感染制御法の開発に向けて~ (Elucidation of mechanism underlying exacerbation of bacterial pneumonia following influenza infection for development of preventive and therapeutic measures against superinfection)
教授 川端 重忠(歯学研究科 微生物学講座) KAWABATA Shigetada(Graduate School of Dentistry)
研究の概要
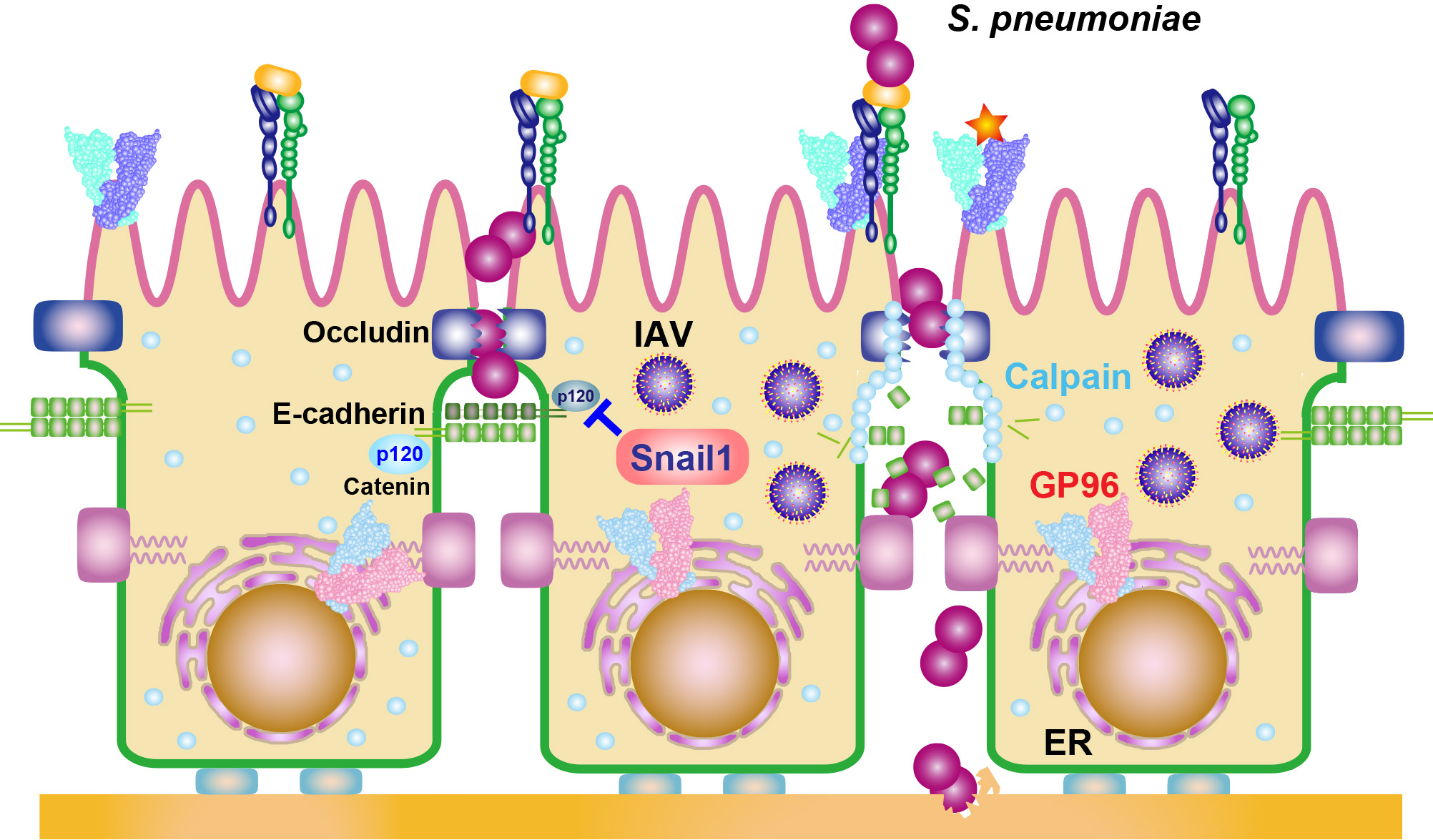
高齢者はインフルエンザなどのウイルス感染症に罹患した後、口腔や鼻咽腔に常在する細菌による細菌性肺炎を合併し、重症化の転帰をたどることが多い。私たちの研究グループは、インフルエンザウイルスに感染した気道上皮細胞では、小胞体局在性の分子シャペロンであるGP96がインテグリンとともに表在化し、肺炎球菌の肺組織への伝播と定着を亢進させることを明らかにした。興味深いことに、GP96のシャペロン機能を標的とする阻害剤の経気道投与により、重複感染マウスにおける肺炎の発症や病態形成は抑制された。すなわち、GP96は肺炎の増悪因子であるとともに、有効な治療標的であることが証明された。さらに、ウイルス感染気道上皮では、細菌の定着が亢進されるだけでなく、細胞間接着分子群の発現抑制を担うSnail1の活性化により、上皮バリアの機能が破綻し、肺炎が重症化することも明らかになった。
研究の背景と結果
インフルエンザは冬期に流行する呼吸器ウイルス感染症であり、日本国内だけでも年間 1,000 万人が罹患し、約 1万人が重症肺炎により死亡する。肺炎の重症化が生じる一因として、鼻咽腔をニッチとする肺炎球菌や口腔細菌による細菌性肺炎の合併が挙げられる。二次性細菌性肺炎の治療には、抗インフルエンザ薬と抗菌薬が併用されるが、使用量の増加に伴う薬剤耐性ウイルス株や耐性細菌株の出現が公衆衛生上の問題である。憂慮すべきは、肺炎による死亡者の95%以上を65歳以上の高齢者が占めることである。高齢化が加速する日本において、薬剤耐性が問題である現行の抗ウイルス薬や抗菌薬とは作用機序が異なり、肺炎の病態生理に基づく新規感染制御法の開発は極めて重要な課題である。
私たち研究グループは、A 型インフルエンザウイルス (IAV) 感染がもたらす気道におけるストレス応答分子群の表在化に着目し、小胞体局在シャペロンであるGP96 がインテグリンとともに感染上気道へ異所性に表出することを明らかにした。二次的に感染する肺炎球菌は、表在化したGP96とインテグリンを宿主レセプターとして、菌体表層に発現するAliA、AliB との相互作用を介して肺組織に伝播し、定着することを証明した ( 図1)。また、GP96 のシャペロン機能を標的とする阻害薬の経気道投与により、重複感染マウスの肺組織への細菌の定着、ならびに炎症細胞の浸潤に伴う組織傷害は著しく抑制された(図2)。
さらに、IAV 感染上皮細胞では、細胞間接着分子群の分解と発現抑制に関与するカルパインやSnail1の活性化より、気道上皮バリアの機能障害が誘導されることが示された。以上の結果から、IAV 感染に伴い気道表層に誘導されるGP96は二次性細菌性肺炎の増悪因子として機能することが明らかになった。また、GP96シャペロン機能の阻害により、細菌性肺炎の発症と病態形成を制御できる可能性が示唆された。
研究の意義と将来展望
超高齢社会が進行する日本において、肺炎により死亡する高齢者の増加が社会的問題になっている。私たちの研究成果により、インフルエンザウイルス感染に伴い誘導されるGP96が肺炎の有望な治療標的であることが証明された。GP96の創薬への応用により、薬剤耐性が問題である既存の抗ウイルス薬や抗菌薬に代わる新たな治療法の開発が期待される。
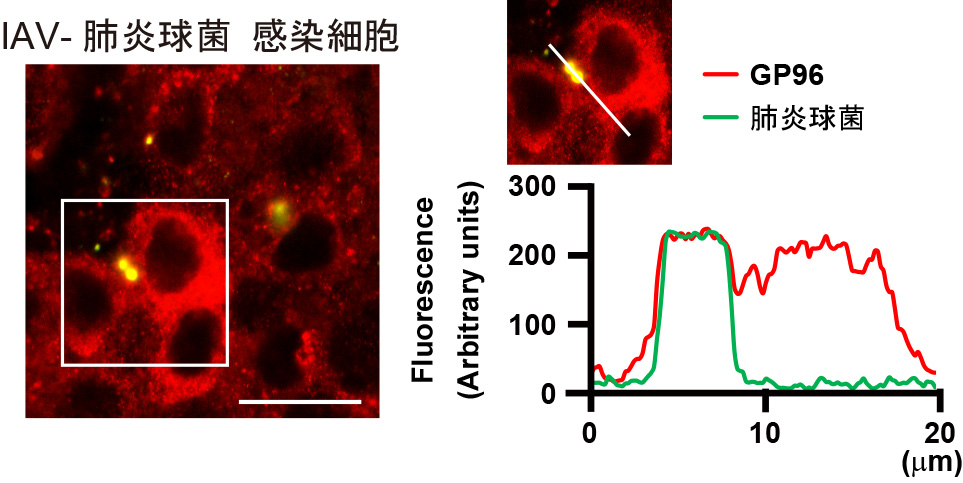
て気道上皮に定着する。
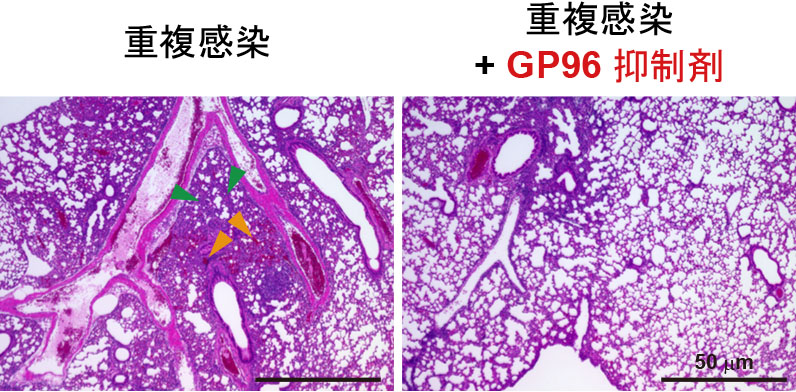
ンジ色の矢尻) が観察されたが、GP96抑制剤の経気道投与により肺炎の病態が
改善した。
担当研究者
教授 川端 重忠(歯学研究科 口腔細菌学教室)
※本学ResOUのホームページ「究みのStoryZ」に、インタビュー記事が掲載されています。是非ご覧ください。
https://resou.osaka-u.ac.jp/ja/story/2018/g008758/
キーワード
インフルエンザ/肺炎球菌/肺炎
応用分野
医療・ヘルスケア/創薬
参考URL
https://resou.osaka-u.ac.jp/ja/research/2021/20210604_1
https://web.dent.osaka-u.ac.jp/mcrbio/index.html
