研究 (Research)
最終更新日:
がん間質をターゲットにした新たな標的アルファ線治療 (Novel targeted alpha therapy against cancer stroma)
助教 渡部 直史(医学系研究科 核医学) WATABE Tadashi(Graduate School of Medicine)
研究の概要
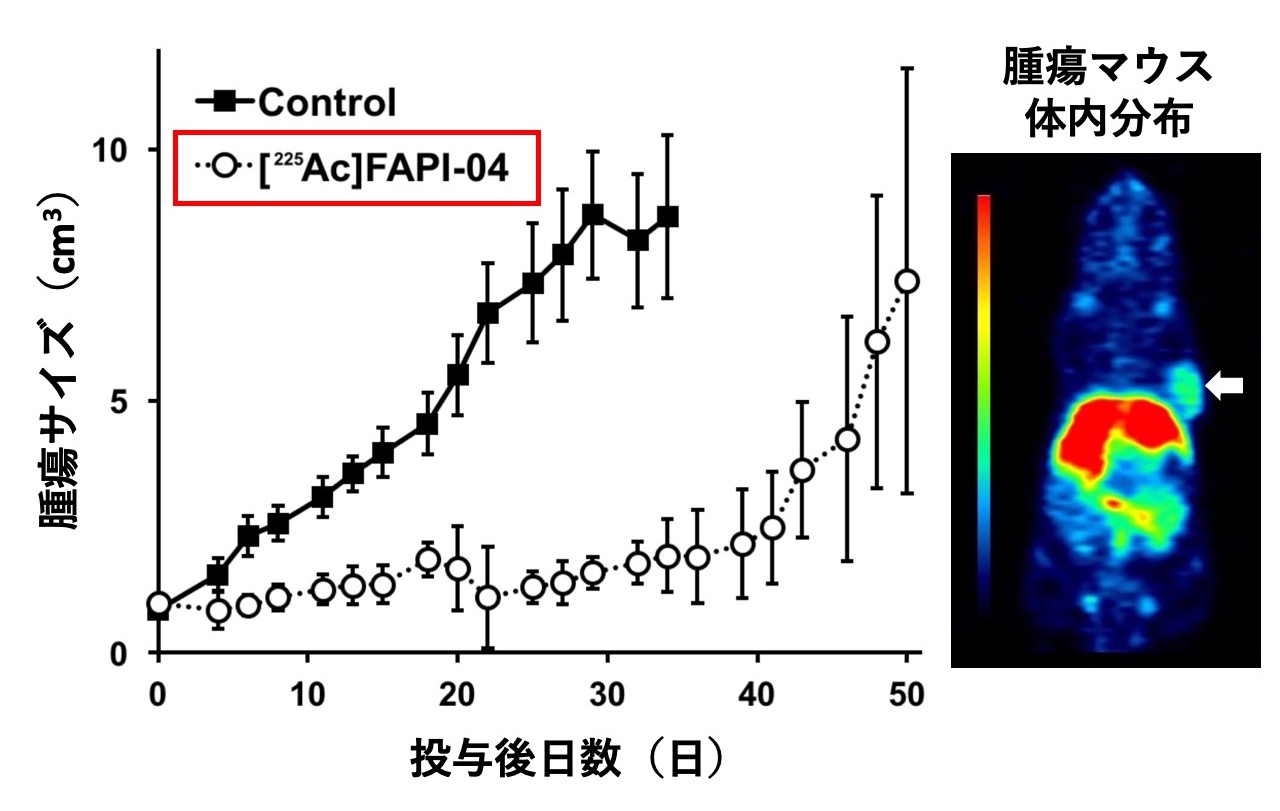
がん間質中のがん関連繊維芽細胞を標的とした新たなコンセプトの放射性治療薬(アクチニウム標識線維芽細胞活性化タンパク質阻害剤([225Ac] FAPI-04))の開発に成功した。本薬を膵臓がんのモデルマウスに投与したところ、腫瘍への選択的集積ならびに良好な増殖抑制効果が確認された(図1)。がん関連繊維芽細胞はがん細胞の増殖に必要な環境を作るとともに、がん細胞に抗がん剤が届くのを防ぐバリアにもなっている。今回、アルファ線と呼ばれる飛程の短い放射線で体内からがんを攻撃することで、がん細胞の増殖を抑制することを世界で初めて示した。今後、通常の治療が効かない難治性の膵臓がんに対する画期的な治療法となることが期待される。
研究の背景と結果
近年、治療効果が高く、周囲の正常細胞への副作用が少ない放射線であるアルファ線を用いた治療が注目を集めている。これまでのアルファ線治療薬はがん細胞表面に現れる特定の分子をターゲットにしてきた。しかし、それらの分子はがん種によって異なることが多く、転移した部位では発現の程度が異なることがあった。またがん細胞を標的とした治療を行うにあたって、がん細胞の周囲に存在する間質がバリアとなって、がん細胞まで抗がん剤が十分に行き渡らないことがあった。特に膵臓がんではこのがん間質の成分が多いため、既存の治療が奏功せずに難治性となることが多く、新たな治療戦略が必要とされていた。今回、独ハイデルベルク大の共同研究によって、がん間質の主要構成成分であるがん関連繊維芽細胞(CAF: cancer associated fibroblast)を標的とした新たな放射性治療薬の開発に成功した。CAFに発現しているFAP(線維芽細胞活性化タンパク質: fibroblast activation protein)は多くのがんの間質に強く発現する一方、正常臓器での発現が低く、FAP標的治療は副作用の少ない画期的な治療となることが期待できる。本研究では、α線放出核種であるアクチニウム(225Ac、半減期:10日)で標識したFAP阻害剤([225Ac] FAPI-04)を膵臓がんモデルマウスの単回静脈内投与を行ったところ、腫瘍選択的に集積し、有意に腫瘍増殖を抑制する効果が認められた。がん細胞の増殖を支えているCAFを標的としてアルファ線で攻撃することで、治療効果が得られることを世界で初めて示した(図2)。現在、大阪大学でも製造可能なα線放出核種のアスタチン(211At、半減期:7.2時間)を用いたFAPIの標識製造にも成功し、有効性を検証している。将来的には膵臓がんを初めとする難治性がんの患者さんにとって、有効な治療薬となることを目指している。
研究の意義と将来展望
がん患者の生存率は全体として上昇傾向にあるが、膵臓がんの5年相対生存率は10%と依然としてかなり低い水準が続いており、既存の治療法の有効性は限られている。本研究成果として開発に成功した[225Ac] FAPI-04は多発転移に対しても投与可能であり、難治性膵がんにおける画期的な治療法となることが期待される。さらにFAPは膵臓がん以外にも多くのがん種で発現していることが報告されており、将来的には他のがん種に対する治療の有効性も検証し、がん種横断的な治療薬として臨床応用を目指したい。
担当研究者
助教 渡部 直史(医学系研究科 核医学)
キーワード
標的アルファ線治療/膵臓がん/がん間質/アクチニウム
応用分野
医療(がん診断・治療)/創薬
