研究 (Research)
最終更新日:
核酸アプタマーを⽤いた軟⾻無形成症治療薬の開発 (Development of oligonucleotide aptamer therapy for achondroplasia )
助教 木村 武司、准教授 窪田 拓生、名誉教授 大薗 恵一(医学系研究科 小児科学) KIMURA Takeshi , KUBOTA Takuo , OZONO Keiichi(Graduate School of Medicine)
研究の概要
軟骨無形成症は四肢短縮型低身長を来す最も頻度の高い骨系統疾患であり、線維芽細胞増殖因子受容体3(FGFR3)遺伝子の機能獲得型変異によって発症します。軟骨無形成症に対する根治療法は現在でも存在しないため、FGFR3の安全かつ効果的な阻害薬が求められてきました。今回我々は、FGFR3のリガンドである FGF2を中和する RNAアプタマー(RBM-007)を開発し、患者由来の疾患特異的 iPS 細胞を用いて有効性を評価しました。
その結果、軟骨分化誘導実験系において RBM-007は in vitro での軟骨分化を回復されることが分かりました。また得られた軟骨組織を免疫不全マウスに移植して内軟骨性骨化を観察する異種移植モデルでも、成長軟骨の形成異常を改善する効果を示しました。モデルマウスや培養細胞系でも同様の効果が確認され、RBM-007が FGFR3阻害薬として機能することを証明することができました。
研究の背景と結果
軟骨無形成症は新生児約 25,000 ⼈に対して1⼈の頻度で発生する、四肢短縮型低身長症の原因として最も頻度の高い骨系統疾患です。線維芽細胞増殖因子受容体3型(FGFR3)遺伝子の機能獲得型変異が原因となって発症することが分かっていますが、 現在まで根本治療法の確立には至っていません。今回、我々は FGFR に結合するリガンドのうち FGF2に着目し、FGF2に特異的に結合・阻害する核酸アプタマーである RBM-007の治療効果について、株式会社リボミック、チェコ共和国 Masaryk 大学医学部の Pavel Krejci 教授の研究チームと共同研究を行いました。
まず、培養細胞株に野生型 / 変異型それぞれの FGFR3を発現させて、FGF2添加によって FGFR3のリン酸化が亢進すること、RBM-007を投与することでそれが低下することを示しました。この結果から、軟骨無形成症において変異 FGFR3がリガンド依存性に活性化されること、FGF2がリガンドとして活性を持つことが示唆されました。更に、培養軟骨細胞と胎生18日のマウス脛骨を用いた実験系で、FGF2を添加すると増殖成長障害を呈すること、RBM-007によってそれが回復することを示し、実際に軟骨細胞 / 組織でも RBM-007が効果を発揮することを明らかにしました。
次に、軟骨無形成症への治療効果を検討するため、患児由来の疾患特異的 iPS 細胞(ACH-iPS)を用いた分化誘導とモデルマウスへの投与実験を実施しました。ACH-iPS は軟骨細胞への分化誘導が障害されることが既報で示されており、その実験系に RBM-007を添加することで正常な軟骨組織を形成することが出来ました。作成した軟骨組織を用いた異種移植モデルでも、RBM-007を投与することで、ACH-iPS由来の成長板軟骨における肥大軟骨細胞径を増大する効果が認められました。また、変異 FGFR3を発現させた ACH モデルマウスと、新たに作成したヒト FGF2過剰発現マウスへの投与実験でも、RBM-007は成長障害を改善する効果を発揮しました。
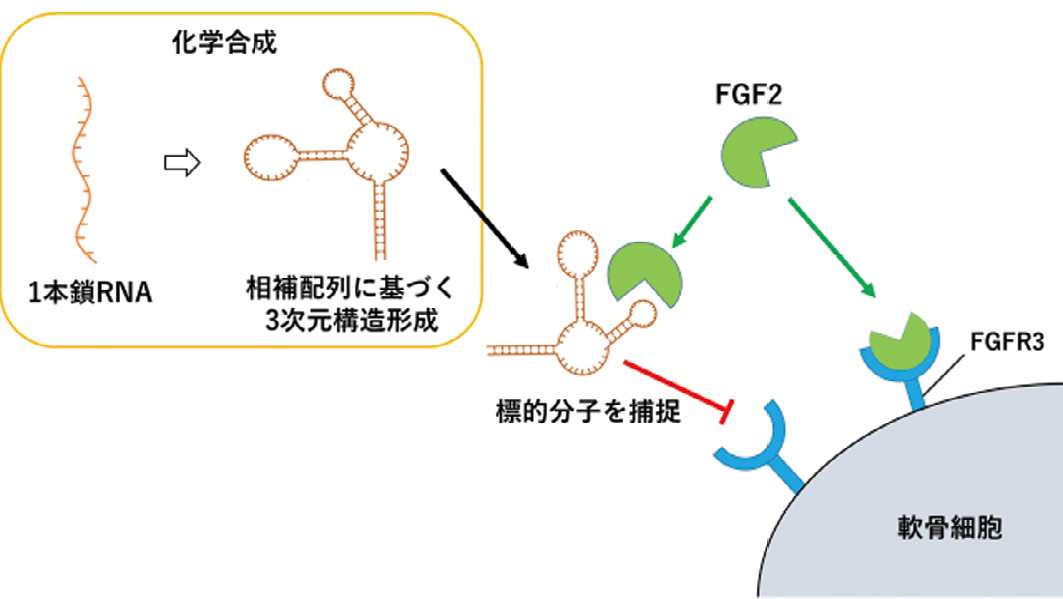
RBM-007は37ヌクレオチドの RNA で構成され、ヒト・マウス・ラット FGF2
と高い特異性・親和性を持って結合できる。生体内で FGF2と FGFR3の結合を
阻害することで、FGFR3シグナルを抑制する。
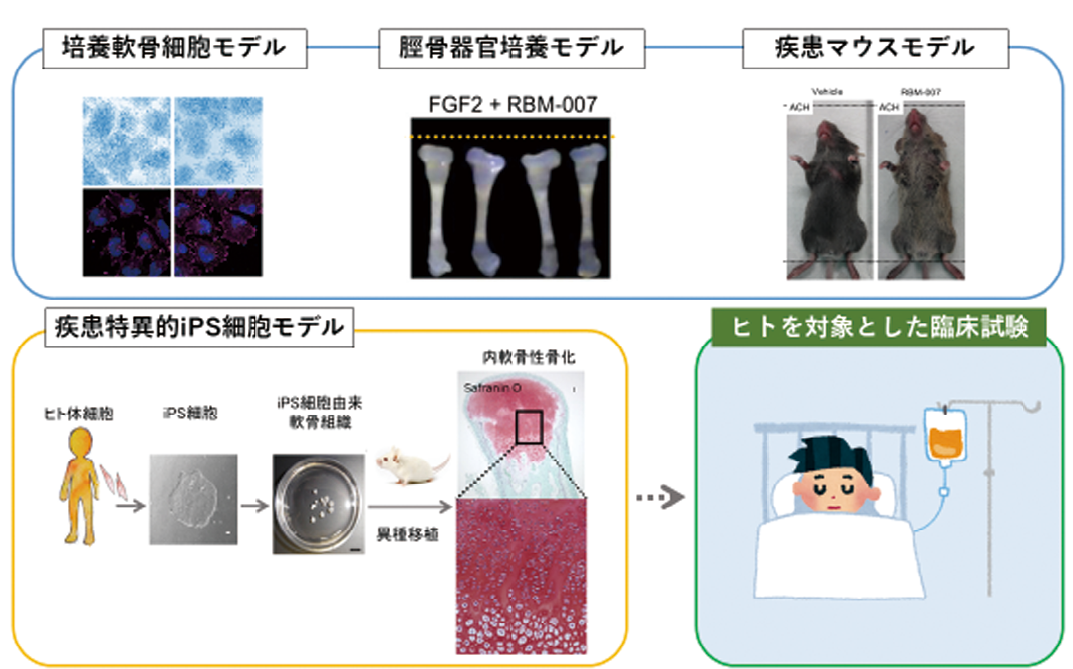
従来の実験動物を用いた細胞、組織、生体での有効性評価に加えて、ヒト iPS 細
胞を用いた疾患モデルでも薬効を確認した。この成果に基づいて、ヒトでの有効
性評価を計画している。
研究の意義と将来展望
本研究において、我々は FGFR3を標的としたリガンド抑制による治療効果を明らかにし、軟骨無形成症やその他の FGFR3関連骨異形成症に対する新規治療法となる可能性を示しました。軟骨無形成症を対象疾患とする RBM-007皮下投与の第1相臨床試験(JapicCTI-205345)は既に完了しており、次の段階である実際の小児患者を対象とした第2相試験について、現在計画しているところです。日本初の新たな核酸医薬として、RBM-007が軟骨無形成症治療の新たな選択肢となることが期待されています。
担当研究者
助教 木村 武司、准教授 窪田 拓生、名誉教授 大薗 恵一(医学系研究科 小児科学)
キーワード
軟骨無形成症/核酸医薬/疾患特異的 iPS 細胞
応用分野
医療・ヘルスケア/創薬
