研究 (Research)
最終更新日:
先制医療技術開発に向けたがん・老化の根本的原理の解明 (Understanding the fundamental principles of aging and cancer for development of the preemptive medicine)
教授 石谷 太(微生物病研究所 生体統御分野) ISHITANI Tohru(Research Institute for Microbial Diseases)
研究の概要
誰もがより長く元気に活躍できる健康長寿社会を実現するためには、がんなどの重大疾病の克服や老化の抑制は重要な課題である。これらの課題に取り組むためには、がん発生や老化の起点となる最初期の原理を明らかにし、そこに介入してこれらを予防するアプローチ、すなわち「先制医療」が有効と考えられる。我々の研究室では、特徴的なモデル生物と最先端の解析技術を駆使して、がんや老化の超初期メカニズムの解明に取り組んでいる。最近では、小型魚類ゼブラフィッシュをモデルとしたイメージング解析により、動物組織が免疫細胞を介さずに前がん細胞を感知して排除する「新たながん抑制メカニズム」を発見し、さらに、このメカニズムの破綻によって初期腫瘍が生じる機序も見出した。また一方で、ヒト老化機構の理解を加速するために、脊椎動物の中で最短の寿命を持つターコイズキリフィッシュ(略称キリフィッシュ)を利用した老化機構高速解析系を独自に構築し、これを駆使して新たな “ 抗老化物質 ” の候補を見出しつつある。
研究の背景と結果
がんの克服は、健康長寿社会実現に向けた重要課題である。がんは治療しても再発の恐れを完全に無くすのは困難であるため、これを克服するためには、発症そのものを予防するアプローチが有効と考えられる。そして、がんを予防する技術を開発するためには、まず、がん発生超初期プロセスを理解し、そこから予防技術のシーズを探索する必要がある。しかしながら、がん発生超初期についての理解は進んでいない。
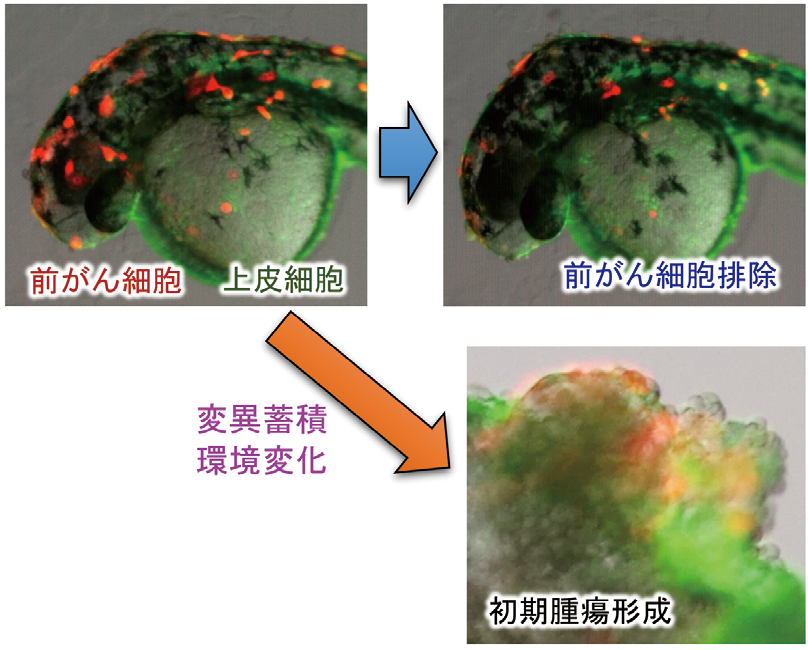
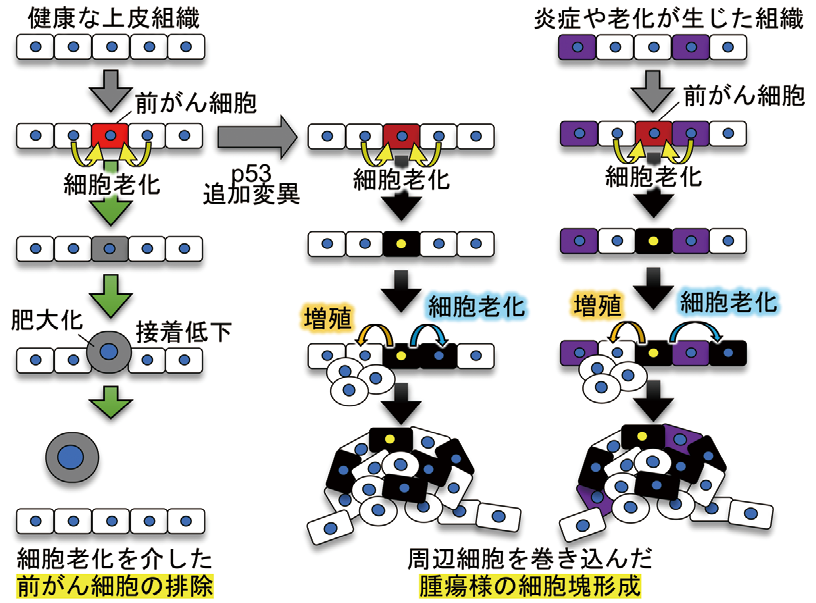
そこで我々は、がん発生超初期のメカニズムを調べるために、イメージング解析に適し、かつヒト同様の脊椎動物である小型魚類ゼブラフィッシュを用いて「生体内に生じた前がん細胞(がんの起源となる変異細胞)の挙動を解析する系」を構築した(図1)。この系を用いた解析により、①健康な上皮組織に単独変異を持つ前がん細胞が生じた際には隣接正常細胞がこれを感知して細胞老化を誘導して体外へ排除すること、②前がん細胞に p53遺伝子変異が追加された場合、あるいは上皮組織に炎症が生じた場合やダメージ細胞(老化様細胞)が多く存在する場合は、前がん細胞は隣接細胞による排除を受け付けずに生存し続け、逆に隣接細胞に老化と増殖を誘導して初期の腫瘍を形成することを発見した(図2;Nature Commun 2019; 2022)。現在、この「がん発生超初期メカニズム可視化解析系」を駆使し、がん発生初期の共通分子基盤の解析と、それに作用する薬剤の探索を進めている。
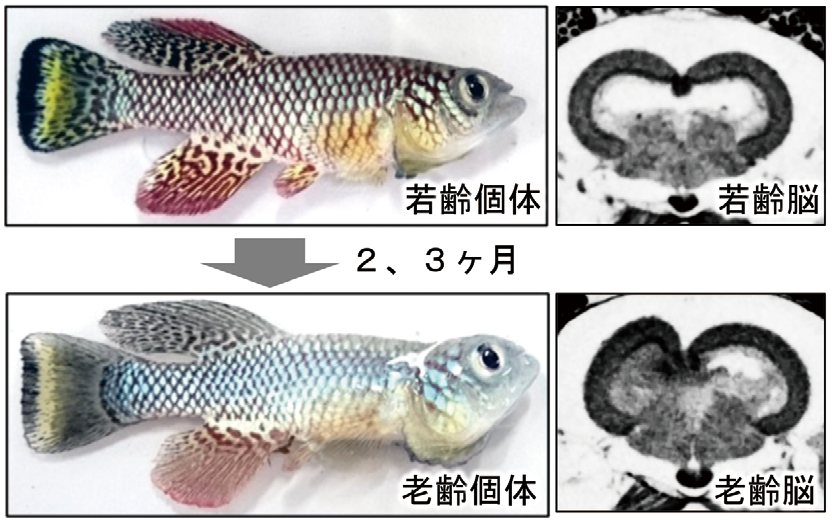
一方で、老化そのものにアプローチする研究も展開している。従来のマウスを用いた老化研究は多数の老化機構を明らかにしてきたが、マウスの老化速度の遅さゆえに研究にかかる時間も長大となっている。そこで我々は、誕生後3ヶ月で急速成長・老化して死に至る特性を持つキリフィッシュ(図3(補足資料))に注目し、その大規模飼育系と高速遺伝子解析法を確立した(Sci Rep 2022)。この技術は、老化研究を大きく加速すると期待されており、事実、我々はすでにこの系を駆使して新たな老化制御機構と抗老化物質を見出しつつある。
系」
研究の意義と将来展望
独自のモデル生物解析系を駆使して、がんや老化の「起こり」を制御する根本的原理を解明したい。そして、独自の発見と解析系を基盤とした異分野連携により、ヒトのがん克服・老化抑制を実現する革新的先制医療技術を確立し、これにより健康長寿社会を実現したい。
担当研究者
教授 石谷 太(微生物病研究所 生体統御分野)
キーワード
がん/老化/先制医療/超初期メカニズム
応用分野
医療・ヘルスケア/創薬
参考URL
https://ishitani-lab.biken.osaka-u.ac.jp/
https://twitter.com/IshitaniLab
http://www.biken.osaka-u.ac.jp/en/achievement/research/2022/178
