研究 (Research)
最終更新日:
量子化学計算による抗体認識メカニズムの解明 (Elucidation of antibody recognition mechanism by quantum chemical calculations)
教授 福澤 薫(薬学研究科 量子生命情報薬学分野) FUKUZAWA Kaori(Graduate School of Pharmaceutical Sciences)
研究の概要
ウイルス感染症やがんの治療に役立つ抗体医薬品の設計のためには、抗原と抗体の相互作用を理解することが重要です。我々は、フラグメント分子軌道(FMO)法という日本発の量子化学計算手法の創薬応用を目指して、産学官連携の「FMO創薬コンソーシアム」を運営しており、抗体設計は重要テーマの1つです。FMO 法では、タンパク質複合体の立体構造に基づいて、アミノ酸残基単位の定量的な相互作用エネルギーを評価し、重要残基を特定することで創薬への糸口を掴むことができます。例えば新型コロナウイルスに関して、スパイクタンパク質と抗体との複合体構造について、12種の抗体との相互作用解析を行ったところ、実験的な活性値(IC50)と良好な相関が得られるとともに、抗体認識部位としてエピトープになり得る9残基の特定に成功しました(図1)。
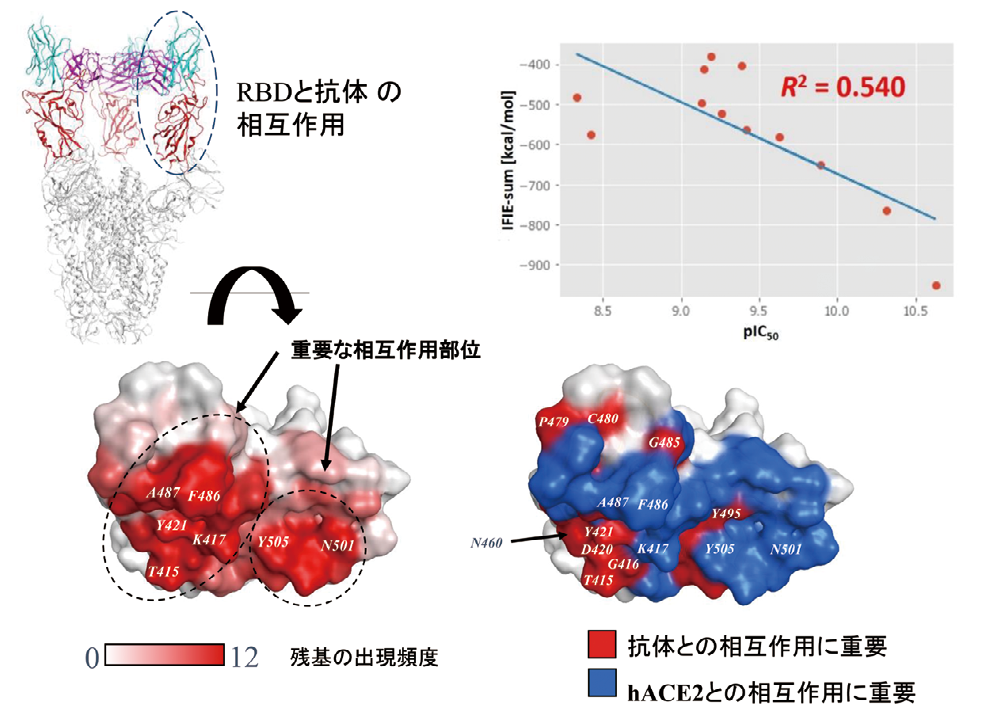
研究の背景と結果
創薬開発においてもデジタル化が進んでいます。計算機を用いた創薬は「インシリコ創薬」と総称されますが、私たちは、原子分子を扱う分子シミュレーション、さらには量子力学に基づく量子化学計算を技術基盤とした研究開発を行っています。FMO 法は、タンパク質などの巨大分子をフラグメント化して扱うことによって、世界的にも類を見ない高速高精度な大規模量子化学計算を実現しています。またフラグメント間の相互作用エネルギーを定量的に評価することができるため、分子間相互作用を理解し、創薬や製剤学の分子設計に活用することができます。FMO 創薬コンソーシアムは、製薬・IT 企業21社と24研究機関が参画しており、FMO 法を実用的な創薬手法として発展させるため に、スー パー コ ン ピュー タ「 富 岳 」を 用 い て( 課 題 番 : 号hp220143)、創薬方法論の開発、創薬応用事例の創出、計算結果の閲覧や解析が可能な FMO データベース(FMODB)の構築および一般公開等の活動を行っています。
新型コロナウイルスにおいては、ウイルス表面のスパイクタンパク質と抗体との複合体構造について、網羅的に FMO 計算を行っています。スパイクタンパク質の受容体結合ドメイン(RBD)と12種の抗体との例では、抗原-抗体結合エネルギーと IC50との間に良好な相関が得られました(R2=0.540)。また、抗体認識部位はヒトの ACE2受容体認識部位と類似しており、全ての複合体において、RBD 表面の特定の9つの残基が、抗体との相互作用の安定化に寄与していることが明らかとなりました(図1)。変異株の解析においても同様のアプローチが可能であり、FMO 法はエピトープ予測に有用であることがわかります。
また、その他の新型コロナウイルス関連タンパク質についても網羅的な FMO 計算結果を FMODB から公開しており、これらをターゲットとした創薬へと繋がることが期待できます(図2)。現在、Protein Data Bank で公開されているさまざまな抗原抗体複合体の FMO 計算を進めており、FMO 計算結果と AI を融合した抗体改変予測へとつながる基礎データを蓄積しています。
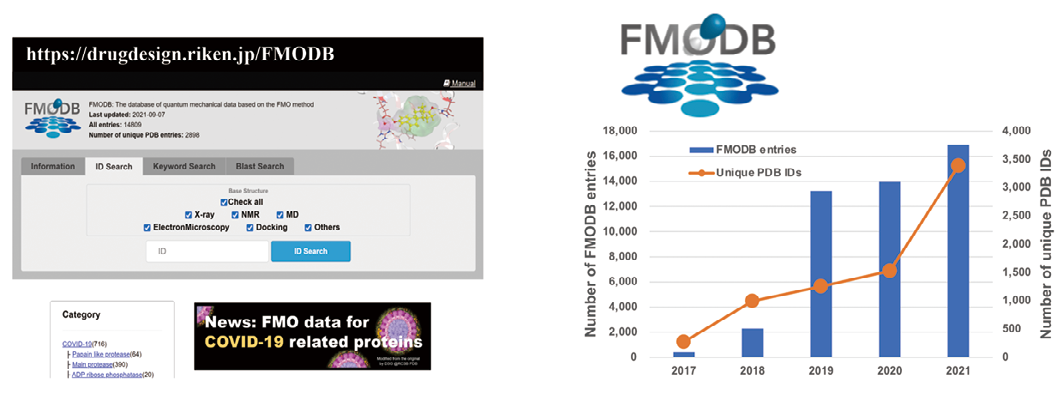
登録構造数の推移(右)
研究の意義と将来展望
現在では、創薬開発に要する膨大な費用と時間を短縮するために、計算科学や AI が随所に活用され始めています。我々の研究は、量子論に基づく精密計算によって疾患に関係する抗体の分子認識メカニズムを解明し、改変抗体の効率的な設計に役立つことが期待されます。また同一の手法をさまざまな創薬モダリティに展開可能であることも大きな特徴です。従来型の低分子創薬のみならず、核酸医薬品や脂質ナノ粒子の設計にも有効な論理的・効率的な分子設計の新領域を切り拓いています。
担当研究者
教授 福澤 薫(薬学研究科 量子生命情報薬学分野)
キーワード
インシリコ創薬/抗体設計/計算構造生命科学/フラグメント分子軌道(FMO)法/スーパーコンピュータ「富岳」
応用分野
創薬/生命科学/抗体設計/データベース
