研究 (Research)
最終更新日:
合成糖鎖を用いたグリココードの解読 (Decoding glycocode using synthetic glycans)
助教 真鍋 良幸、教授 深瀬 浩一(理学研究科 化学専攻) MANABE Yoshiyuki , FUKASE Koichi(Graduate School of Science)
研究の概要
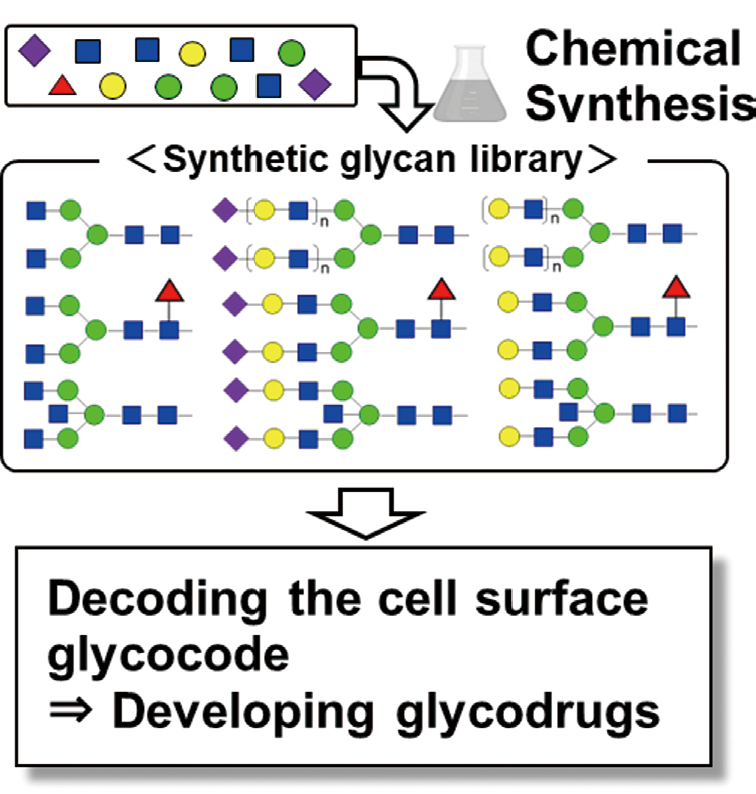
糖鎖は、核酸、タンパク質に続く第3の生命鎖と呼ばれ、多くの生命現象に関与する。特に、糖鎖は細胞を覆うように存在することから、外界とのファーストコンタクトの場を提供し、感染症、免疫応答、細胞間コミュニケーションなど、自己・非自己の認識に重要である。しかし、糖鎖は、非鋳型的に数百の酵素を介して生合成されるため、多様かつ不均一性な構造を持ち、分子レベルでの機能解析・制御はほとんど進んでおらず、医薬等への応用も限られている。そこで我々の研究グループは、合成生物学的アプローチで、細胞表層の糖鎖情報(グリココード)を読み解き、利用する研究を進めている(図1)。特に、代表的な翻訳後修飾糖鎖であるN – グリカンを対象とし、その実践的な合成法を確立し(図2)、合成N – グリカンを用いた分子レベルでの機能解析に着手している。
研究の背景と結果
N -グリカンは、多様な構造を持ち、その構造に基づいた機能を有する。シアル酸は、非還元末端に存在し、細胞の外側に位置するため、病原体の認識サイトとなりやすく、感染症と深く関連する他、その認識レクチン(シグレック)との相互作用を介して、免疫制御に深くかかわる。我々はN – グリカンの化学合成研究と構造に基づいた機能研究に取り組んできた。
例えば、我々は真菌に対する防御に働くタンパク質デクチン1が、コアフコースと呼ばれるN – グリカン修飾糖鎖構造を持つ免疫グロブリン G を認識することを見出した。N – グリカン合成では、分枝構造の構築がカギとなる。我々は、分枝マンノースの3位と6位に非還元末端フラグメントをそれぞれグリコシル化する収束的なルートを採用した。このグリコシル化は、大きなフラグメント同士を立体的に込み合った位置で連結するため、多くの困難が伴ったが、エーテル溶媒を用いたカチオン中間体の配位安定化、遠隔位アシル基の配位を利用した立体制御(遠隔基関与)を見出し、高い収率、立体選択性を実現した。これより、N – グリカンの実践的合成が可能となった。ここでは、インフルエンザウイルスの表面に存在し、感染細胞から遊離する際に機能するノイラミニダーゼ(非還元末端シアル酸の切断酵素)と対象とし、この酵素がN – グリカン上のシアル酸を認識する分子基盤を解析した(図3)。
具体的には、N – グリカンの非還元末端の分枝鎖の認識の違いについて調べるために、片方の分枝鎖のみを重水素で標識した1、2を合成した。加えて、分枝数(=シアル酸の数)がノイラミニダーゼ認識に与える影響を評価するために、4分枝N – グリカン3を合成した。
これらの合成糖鎖を用いた解析の結果、ノイラミニダーゼが下側の分枝鎖のシアル酸を優先すること、また、分枝数はノイラミニダーゼによる基質認識にほとんど影響を及ぼさないことが明らかになった。


研究の意義と将来展望
糖鎖は、多くの疾病と深くかかわっている。例えば、多くの疾患は恒常性の乱れが原因となっており、糖鎖はその維持に重要な役割を果たす。そのため、糖鎖は、診断のバイオマーカーとして汎用されている。グリココードの分子レベルでの理解が進めば、がんや免疫疾患、神経疾患などの疾患における恒常性の乱れを正常な状態へと戻すアプローチが可能になる。このように糖鎖に着目することで、新たな概念に基づく革新的な医薬品開発につながると期待している。
担当研究者
助教 真鍋 良幸、教授 深瀬 浩一(理学研究科 化学専攻)
※本学ResOUのホームページ「究みのStoryZ」に、インタビュー記事が掲載されています。是非ご覧ください。
深瀬 浩一
https://resou.osaka-u.ac.jp/ja/story/2017/g004362/
https://resou.osaka-u.ac.jp/ja/story/2017/g004361/
キーワード
グリココード/糖鎖合成/糖鎖/N – グリカン/免疫
応用分野
医療・ヘルスケア/創薬
