研究 (Research)
最終更新日:
がん微小環境に着目した肝がん進展機序の解明と臨床応用 (Elucidation of the mechanism of liver cancer progression focusing on tumor microenvironment and its clinical application)
講師 疋田 隼人、教授 竹原 徹郎(医学系研究科 消化器内科学) HIKITA Hayato , TAKEHARA Tetsuo(Graduate School of Medicine)
研究の概要
がん組織にはがん細胞だけでなく、免疫細胞・線維芽細胞・血管内皮細胞など様々な間質の細胞が存在します。これらの細胞は、がん細胞と相互作用することで、がんの進展に有利な環境を形成しており、このような環境をがん微小環境と呼びます。我々は、がん微小環境における肝がん進展分子機序の解明に取り組んでいます。これまで、肝がん微小環境において、GDF15(論文3)、IL-6ファミリーサイトカイン(論文1)、CTGF(論文1、4)が肝がん細胞と間質の細胞との相互作用に重要な分子であることを見出し、報告してきました。
一方、将来の肝発がんリスクが高い患者と低い患者を層別化する新しいバイオマーカーの開発にも取り組んでいます。肝がん微小環境で発見した GDF15は、慢性肝疾患患者の血液中で上昇していることを見出しました。血液中の GDF15が高い患者は、C 型肝炎ウイルスを除去しても肝がんに進展しやすいことを発見し、GDF15は肝発がんリスクを層別化する新しいバイオマーカーになることを報告しました(論文2)。
研究の背景と結果
肝がんの多くは、C 型肝炎、B 型肝炎、非アルコール性脂肪性肝疾患(NAFLD)などの慢性肝疾患の患者さんから発症します。肝がんは、現在国内においてがんによる死亡原因のうち第5位となっている極めて予後不良な疾患です。
肝細胞がんを含む多くのがんではがん細胞を取り巻く免疫細胞・線維芽細胞・血管内皮細胞といった間質の細胞とがん細胞そのものが相互作用を介し、がん微小環境を形成してがんの発展を促進させます。しかし、肝臓において線維化の中心的役割を担う肝星細胞が、肝がん微小環境において、どのようにがん細胞と相互作用を有するのかはわかっていませんでした。
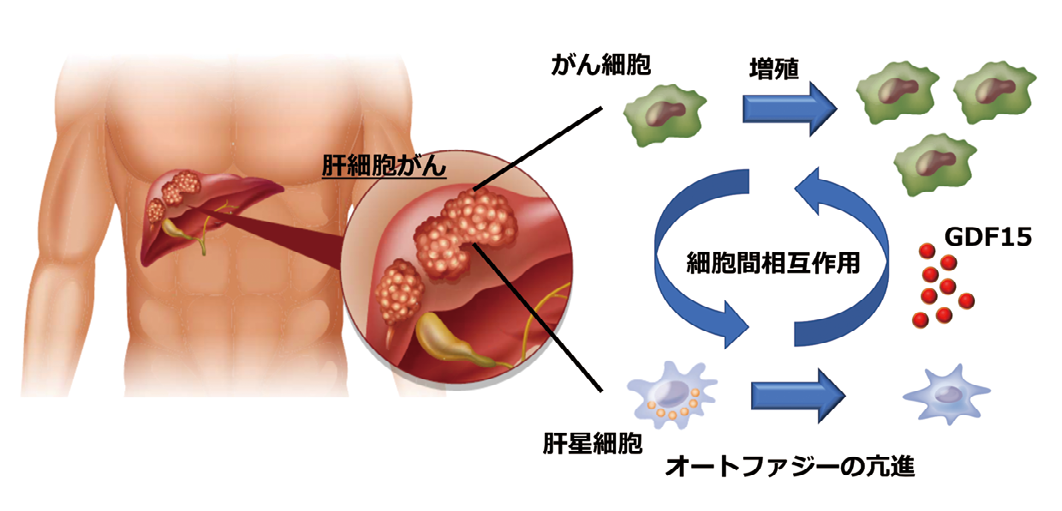
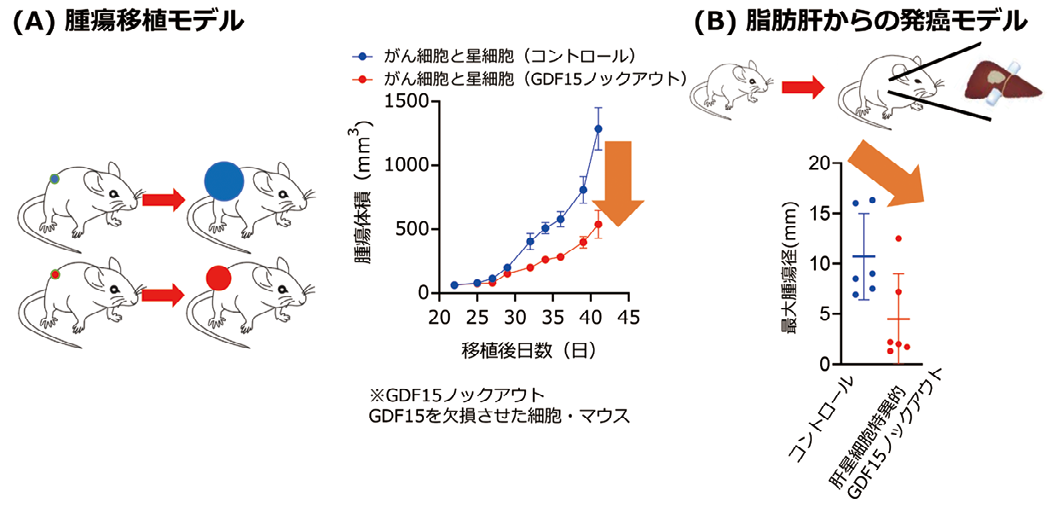
我々は、肝がん微小環境では、肝がん細胞により肝星細胞のオートファジー*1が促進し、オートファジー促進を介して肝星細胞から GDF15が分泌され、肝がん細胞の増殖が促進されることを見出しました(図1)。腫瘍移植モデルや肝発癌モデルマウスで肝星細胞の GDF15を欠損させると肝がん進展は抑制され、GDF15は肝癌の新しい治療標的になることを発見しました(図2)。ヒト肝癌切除検体から単一細胞解析を行い、肝がん微小環境に GDF15を発現する肝星細胞が存在することを見出し、血液中の GDF15濃度が高い肝細胞がん患者さんは予後が悪いことも明らかにしました (論文3)。
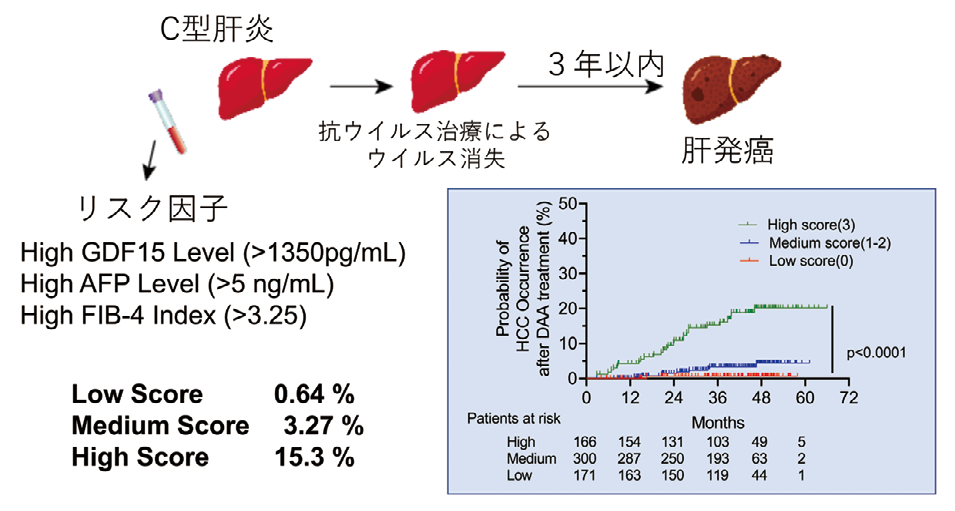
一方、C 型肝炎は飲み薬でウイルスを除去することが可能となり、ウイルスを除去することで肝がんに進行することが抑制できるようになりました。しかし、中にはウイルスを除去しても肝がんに進行することがあります。今回肝発癌前の慢性患者の血液中でも GDF15が高いことを見出しました(論文2)。興味深いことに、血液中の GDF15高いことは、血液中の AFP が高いこと、肝臓の硬さの指標である FIB-4 index *2が高いことととは独立したウイルス消失後の肝発がんのリスク因子であることを発見し(図3)、GDF15が新たな肝発がん予測バイオマーカーとして利用できることを報告しました(論文3)。
*1 細胞が自らの細胞質の一部を分解し、アミノ酸などを再生する機構。近年がんとの関連も報告されている。
*2 C型肝炎や非アルコール性脂肪性肝疾患において、肝臓の硬さと相関すると報告されている指標。血清 AST 値、血清 ALT 値、血小板数及び年齢から算出される。
研究の意義と将来展望
肝がん患者に対して、がん微小環境を治療標的とした新たな治療法の開発が期待されます。慢性肝疾患患者に対して、肝発がん高リスク患者絞り込みの新規バイオマーカーの確立が期待され、効率的な肝がん早期発見スクリーニング法の確立が期待されます。
担当研究者
講師 疋田 隼人、教授 竹原 徹郎(医学系研究科 消化器内科学)
※本学ResOUのホームページ「究みのStoryZ」に、インタビュー記事が掲載されています。是非ご覧ください。
竹原 徹郎
https://resou.osaka-u.ac.jp/ja/story/2022/nl87_mimiyori_vol10/
キーワード
肝がん/がん微小環境/慢性肝炎/GDF15/CTGF
応用分野
創薬/バイオマーカー
