研究 (Research)
最終更新日:
糖鎖抗原を用いた革新的がん免疫療法の開発 (Development of Innovative Cancer Immunotherapy Using Antigen Glycans)
助教 真鍋 良幸、教授 深瀬 浩一(理学研究科 化学専攻 ) MANABE Yoshiyuki , FUKASE Koichi (Graduate School of Science)
研究の概要
糖鎖は、核酸、タンパク質に続く第3の生命鎖と呼ばれ、多くの生命現象に関与する。特に、糖鎖は細胞を覆うように存在することから、外界とのファーストコンタクトの場を提供し、感染症、免疫応答、細胞間コミュニケーションなど、自己・非自己の認識に重要である。しかし、糖鎖は、非鋳型的に数百の酵素を介して生合成されるため、多様かつ不均一性な構造を持ち、分子レベルでの機能解析が進んでおらず、医薬等への応用も限られている。そこで我々の研究グループは、化学的アプローチで、細胞表層の糖鎖を編集し、その機能を利用する研究を進めている。本研究では体内に大量の自然抗体が存在する糖鎖をがん細胞表層に導入することで、がんに対して免疫反応を誘導することに成功した。さらに、この際、糖鎖を光で開裂可能な保護基で暫定的に保護することで(ケージド戦略)、光照射による免疫反応誘導のスイッチングを可能にした。
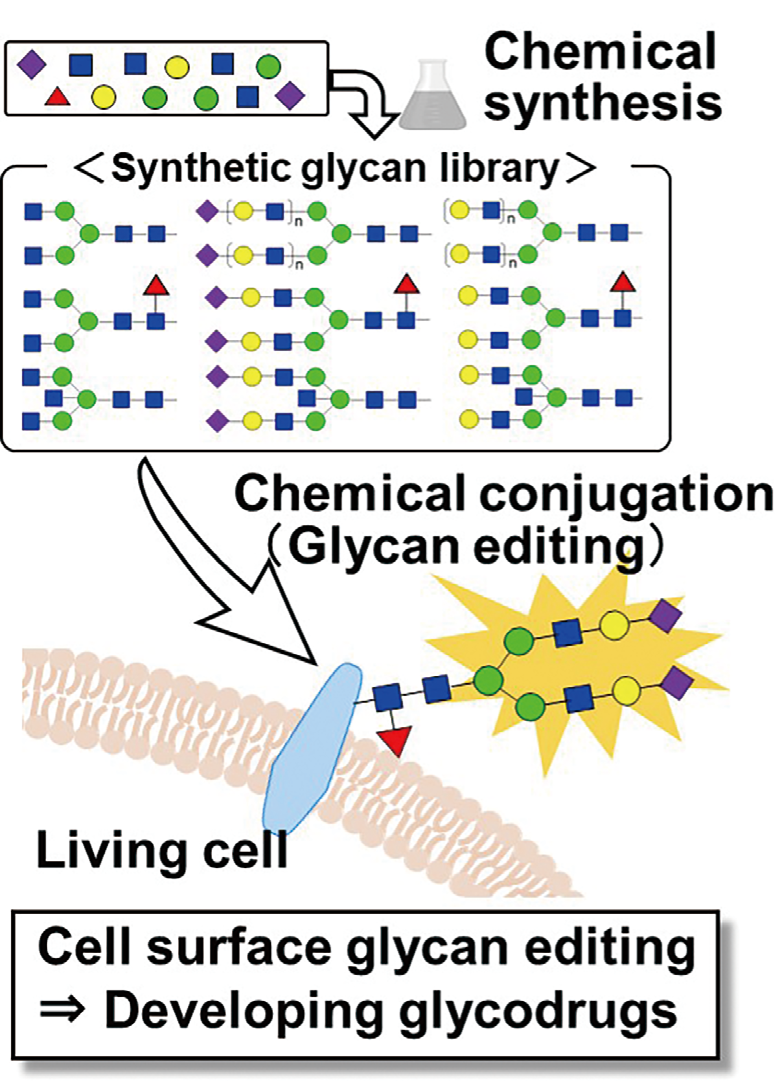
研究の背景と結果
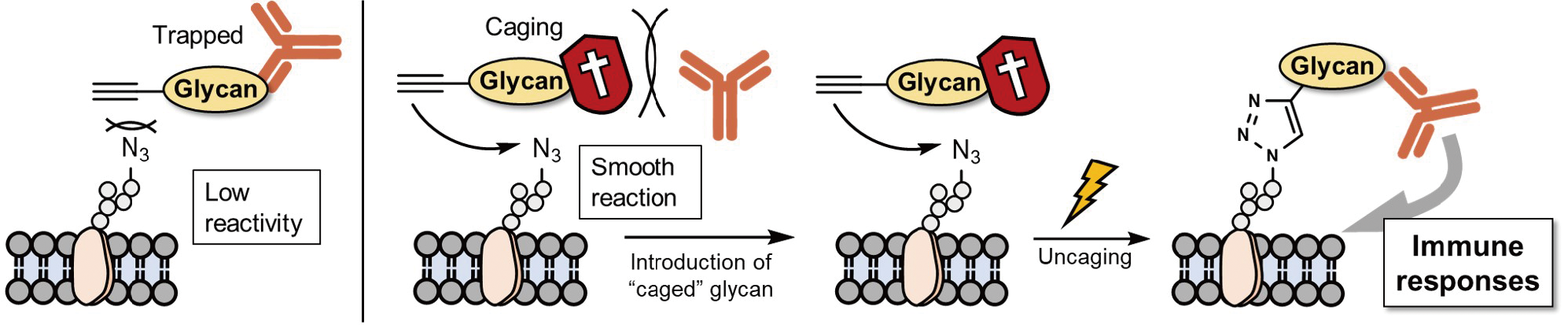
糖鎖は細胞表面を覆うように存在し、自己・非自己を識別する目印としての役割を果たす。α -gal(3糖構造)やα – ラムノース(α -Rha)などの糖鎖抗原は、バクテリアなど自然界の多くの生物が持つものの、ヒトはこの糖鎖を持たず、代わりにこの糖鎖に対する自然抗体を大量に持つ。すなわち、糖鎖抗原は非自己の目印として働き、激しい免疫反応を誘起する。本研究では、これをがん免疫療法に利用した。すなわち、がん細胞表層に糖鎖抗原を導入することで、体内の自然抗体をリクルートし、がんに対して免疫反応を誘導した。このような手法は抗体リクルート戦略として、注目を集め、我々はα -gal とがんを認識する抗体を複合化することで、がん細胞への抗体リクルートに成功していた。本研究においては、アジド糖を用いた代謝標識によりがん細胞表層をアジド標識し、click chemistry によりα -Rha を導入し、免疫反応を誘導した。この際、光により開裂可能な保護基で暫定的に保護したα -Rha(ケージドα -Rha)を用い、任意のタイミングで、光照射によって活性を引き出すケージド戦略を組み合わせて利用することで、抗体リクルート戦略の実用性を大きく高めた。本戦略を用いることで、生体内に存在する抗体によるα -Rha の捕捉を防ぎ、速やかに細胞表層に糖鎖を導入することに成功した。さらに、光照射で活性のスイッチングが可能で、自在に時空間制御しながら免疫応答を誘導できた。糖鎖が、レクチンや抗体など生体内に遍在するさまざまな生体分子との相互作用を通じて機能していることを考えると、このような相互作用を時空間的に制御することは、糖鎖機能を引き出すために不可欠で、本研究では、その方法論を提示することに成功した。
研究の意義と将来展望
細胞を覆う糖鎖は、多くの生体分子と相互作用し生命現象に関与する。この細胞表層の糖鎖構造を編集する技術は、免疫、細胞間コミュニケーション、シグナル伝達など、生体膜上での現象を制御する新しい手法を提案するものである。本研究では、糖の代謝標識とケージド戦略を組み合わせて用いた汎用性の高い細胞表層糖鎖の機能制御法を提案した。本戦略により、細胞表層の糖鎖機能の実用的な機能制御が可能となり、将来的に糖鎖医薬実現につながることを期待している。
担当研究者
助教 真鍋 良幸、教授 深瀬 浩一(理学研究科 化学専攻)
キーワード
糖鎖/抗体/免疫/光スイッチング
応用分野
医療・ヘルスケア/創薬
参考URL
https://researchmap.jp/researchmap_manabe
https://researchmap.jp/read0076573
