研究 (Research)
最終更新日:
安全で有効なアンチセンス核酸医薬の開発に向けて (Towards the development of safe and effective therapeutic antisense oligonucleotides )
講師 山口 卓男、教授 小比賀 聡 (薬学研究科 生物有機化学分野) YAMAGUCHI Takao , OBIKA Satoshi (Graduate School of Pharmaceutical Sciences)
研究の概要
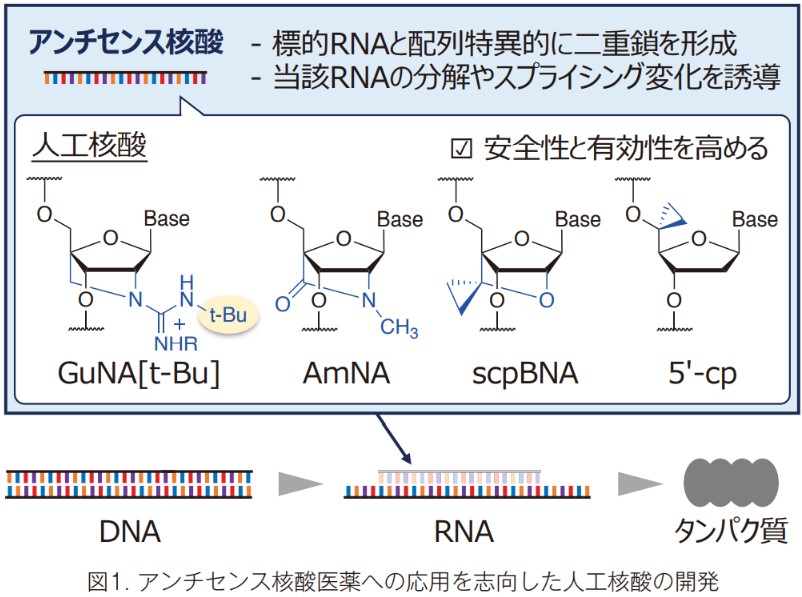
アンチセンス核酸は、治療標的の RNAと配列特異的に二重鎖を形成するようデザインされたオリゴ核酸です。例えば、疾患原因になっている mRNA の発現量を減少させたり、pre-mRNA のスプライシングに変化を与えて望みのタンパク質の発現量を増加させたりといった創薬アプローチが可能で、2023年9月現在、10品目が医薬承認を受けるまでに成長しています。データベース化されている mRNA や pre-mRNA の配列情報に基づいて、迅速に医薬開発できる点が大きな特徴になっています。我々の研究室では、アンチセンス核酸の安全性や有効性を高めることを目標として、材料となる人工核酸(モノマー分子)の開発に取り組んできました。これまで、GuNA[t-Bu] や AmNA、scpBNA、5′-cp といった従来のものよりも高機能な人工核酸の開発に成功しており、アンチセンス核酸へとそれらを搭載することで医薬応用化を進めています。
研究の背景と結果
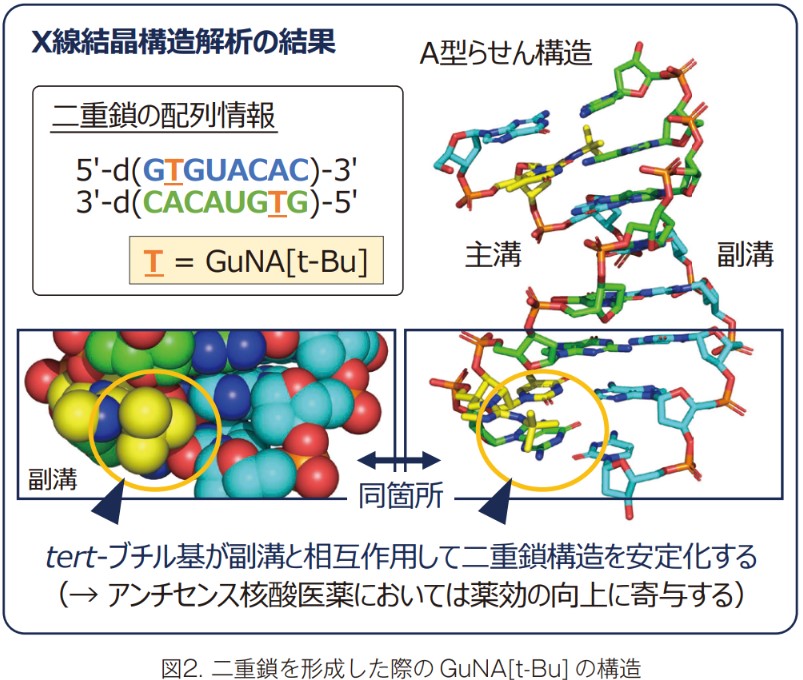
アンチセンス核酸は、投与後に様々な核酸分解酵素の認識をかい潜りながら、疾患の臓器・組織へと辿り着きます。そして、臓器・組織の細胞内へと侵入し、標的 RNA と配列特異的に二重鎖を形成することで、薬効へと繋がっていきます。このような過程を経ることから、アンチセンス核酸においては「核酸分解酵素に対する安定性」や「標的RNA に対する二重鎖形成能」が重要な性質となってきます。我々は、これら2つの性質を向上させるような人工核酸を多数開発し、アンチセンス核酸への応用化を進めてきました。例えば、AmNA やscpBNA はこれら2つの性質を大きく向上させる人工核酸として開発してきたもので、アンチセンス核酸の薬効を飛躍的に高めることが可能です。また、5′-cp は核酸分解酵素に対する安定性を高める人工核酸で、アンチセンス核酸の安全性も向上させるといった特徴を持ちます。最近の研究では、嵩高いtert-ブチル基を有する GuNA[t-Bu] が標的RNAに対する二重鎖形成能を飛躍的に高めるということを見出しました。二重鎖の X 線結晶構造解析を行った結果、GuNA[t-Bu] のtert-ブチル基は副溝に綺麗にはまり込んでいることが分かりました。この結果から、GuNA[t-Bu] のtert-ブチル基と副溝の間に働く相互作用によって標的RNA に対する二重鎖形成能が高まるということが明らかになりました。なお、アンチセンス核酸に GuNA[t-Bu] を導入することで核酸分解酵素に対する安定性も大きく向上します。核酸分解酵素に対する安定性と二重鎖形成能を向上させる GuNA[t-Bu] は、アンチセンス核酸の優れた材料と言えます。ここで紹介した4つ人工核酸(GuNA[t-Bu]、AmNA、scpBNA、5′-cp)については、供給体制の構築も進めています。アンチセンス核酸をはじめとする核酸医薬の開発において、これら人工核酸が役立つことを期待しています。
研究の意義と将来展望
低分子医薬や抗体医薬で治療が困難な遺伝性疾患等を対象として、アンチセンス核酸による治療薬開発が活発化しています。我々が開発してきた人工核酸は、アンチセンス核酸の安全性や有効性を高めるといった優れた特徴を有しています。共同研究等を通じて、これら人工核酸技術の社会実装を積極的に進めており、患者さんへと1日でも早く良い薬を届けたいと考えています。
担当研究者
講師 山口 卓男、教授 小比賀 聡(薬学研究科 生物有機化学分野)
キーワード
アンチセンス/核酸医薬/創薬/RNA/DNA
応用分野
医療・ヘルスケア/創薬
参考URL
https://www.phs.osaka-u.ac.jp/homepage/b007/
https://researchmap.jp/takao-yamaguchi
https://researchmap.jp/read0014368
