研究 (Research)
最終更新日:
革新的がんワクチン開発を目指して (Development of innovative cancer vaccines)
准教授 真鍋 良幸 (理学研究科 化学専攻)、特任教授(常勤) 深瀬 浩一(放射線科学基盤機構) MANABE Yoshiyuki (Graduate School of Science), FUKASE Koichi (Institute for Radiation Sciences)
研究の概要
抗原とアジュバント(免疫賦活化剤)を複合化/共集積化させたセルフアジュバンティングワクチンは、抗原特異的な免疫応答を実現できる。我々は、本戦略によるがんワクチンの開発を目指している。
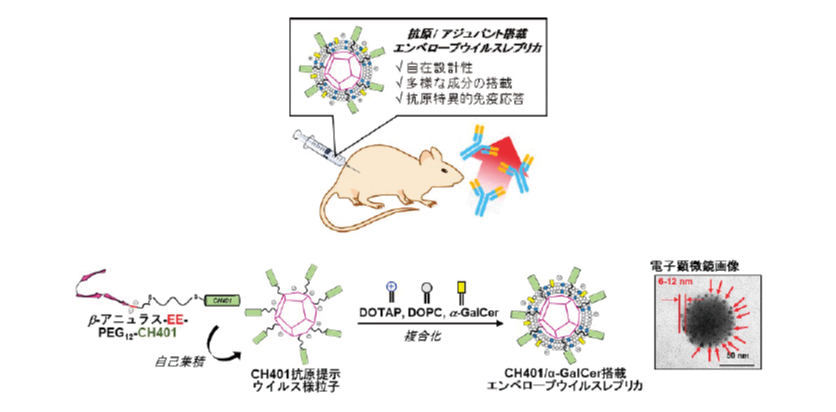
本研究では、新たなセルフアジュバンティングワクチンとして、乳がん抗原である CH401ペプチドとアジュバントであるα – ガラクトシルセラミド(α -GalCer)の両方を提示した人工エンベロープウイルスレプリカを設計・合成し、その機能を評価した。この CH401/α -GalCer搭載エンベロープウイルスレプリカは、完全化学合成により調製可能で、狙い通り、搭載した CH401抗原に対する免疫応答を特異的に誘導した。
本ワクチンマテリアルの特徴は、その設計性の高さで、多様な免疫誘導因子を抗原と共搭載可能で、抗原特異的な免疫応答の精密制御を実現できる。
研究の背景と結果
がんワクチン療法は、転移がんなどの手術が不可能ながんも治療でき、しかも再発を抑える理想的な治療法になり得る。しかし、がん患者は免疫不全を起こしていることが多く、また、がんが免疫回避機構を備えていることもあり、高い効果を持つがんワクチンの開発は困難である。加えて、過剰な免疫反応の誘導は重篤な副作用につながる懸念もある。そのため、現状では、がんワクチンは標準的な治療法としては確立されていない。我々は、この問題を打破する画期的なワクチン戦略として、セルフアジュバンティングワクチンに注目している、
この手法では、抗原とアジュバントを複合化/共集積化することで、同一の免疫細胞に作用させ、抗原特異的な免疫反応を効果的に誘導できる。そのため、副作用を抑えつつ、高い効果が期待できる。本研究では、完全化学合成により調製可能なウイルス用粒子をがん抗原ペプチドのキャリアとして利用した新たなセルフアジュバンティングワクチンを開発した。まず、乳がん抗原(CH401 ペプチド)をウイルス骨格を形成する自己組織化ペプチドと複合化し、CH401抗原を提示した人工ウイルス様粒子を構築した。さらに、これを糖脂質アジュバント(α -GalCer)を含む脂質二重膜で覆うことで、抗原/アジュバント搭載エンベロープウイルスレプリカの調製に成功した。
このウイルス用粒子は、高い安定性を示し、さらに、免疫細胞に速やかに取り込まれた。これを in vivo 系でマウスに免疫したところ、狙い通り、CH401抗原に対する免疫応答を特異的に誘導した。このように、今回の抗原 / アジュバント搭載エンベロープウイルスレプリカは、搭載した抗原に対する免疫応答を効果的に誘導できる優れたワクチンマテリアルであることが証明された。
研究の意義と将来展望
生体材料をそのまま用いる生ワクチン、不活化ワクチンは効果的に免疫反応を誘導できるが、副作用も大きい。一方で、ワクチンに必要な成分を抽出して利用する成分ワクチンは、安全性は高いものの、その効果は限定的である場合が多い。
本研究では、完全化学合成によりウイルス用粒子を構築し、これが効果的に免疫応答を誘導することを示した。本研究は、高い安全性と効果を両立する革新的なワクチン創製につながると期待している。
担当研究者
准教授 真鍋 良幸 (理学研究科 化学専攻)、特任教授(常勤) 深瀬 浩一(放射線科学基盤機構)
キーワード
ワクチン/免疫/自己組織化/ペプチド
応用分野
医療・ヘルスケア、創薬
参考URL
https://researchmap.jp/researchmap_manabe
https://researchmap.jp/read0076573
