研究 (Research)
最終更新日:
がん細胞に核酸医薬を効率よく取り込ませる新技術―新規TRPC3/C6(Transient Receptor Potential C3/C6)チャネル選択的活性化剤L687によるアンチセンス核酸の細胞内取り込み亢進― (A new technology for intracellular uptake of oligonucleotide therapeutics into cancer cells- A novel TRPC3/TRPC6)
教授 小比賀 聡 (薬学研究科 生物有機化学分野)、准教授 下條 正仁(薬学研究科 生物有機化学分野)、特任准教授 永田 龍 (薬学研究科 生物有機化学分野) OBIKA Satoshi (Graduate School of Pharmaceutical Sciences), SHIMOJO Masahito (Graduate School of Pharmaceutical Sciences), NAGATA Ryu (Graduate School of Pharmaceutical Sciences)
研究の概要
アンチセンス核酸(ASO)などの核酸医薬の分野では、核酸医薬を如何に標的組織に送達し、如何に選択的に標的細胞内に取り込ませるかが困難な課題となっており、それが特にがん疾患治療を目指す核酸医薬の実用化の妨げになっています。私たちは、以前に見出していた培地の Ca2+ 濃度を上げると ASO の細胞内取り込み量が上昇するという知見を基に、肺がん細胞で高発現している TRPC3/C6チャネルという Ca2+ 透過型のチャネルに着目し、これらを活性化することで、ASOの細胞内取り込み量を上げることができるのではないかと考えました。実際、肺がん由来の細胞に新たに見出した新規低分子 TRPC3/C6活性化剤 L687と ASO を同時に添加したところ、ASO の細胞内取り込み量が L687無添加の場合と比べて、大きく上昇することを見出しました。担がんマウスを用いた動物実験では、L687と ASO を併用すると ASO単独投与群と比較して腫瘍内の ASO 量が増加し、標的遺伝子の発現が減少し、腫瘍サイズの増大が有意に抑制されました。
研究の背景と結果
ASO 等の核酸医薬は、低分子医薬や抗体医薬と異なり、遺伝子レベルで疾患タンパク質の発現を制御でき、様々な難治性希少疾患治療薬として実用化されています。この特性は、がん疾患への臨床応用も期待でき、実際に今までに数多くの ASO を含む様々な核酸医薬についてがん疾患を適応症とする臨床試験が進められてきました。しかしながら、2024年10月現在、承認申請に至ったがん適応核酸医薬品は、低リスク骨髄異形成症候群適応の1剤を除いてなく、臨床後期段階まで進んだものもほとんどありません。全身投与した核酸医薬をがん組織に送達しがん細胞内に取り込ませるための適切な手段(Drug Delivery System, DDS)がいまだに存在しないことが、その理由と考えられます。
当研究室では Ca2+ が核酸医薬の細胞内移行性に関与する可能性を示してきており、今回ある種のがん細胞に多く発現する Ca2+ 透過型のTRPC3/C6チャネルに着目しました。
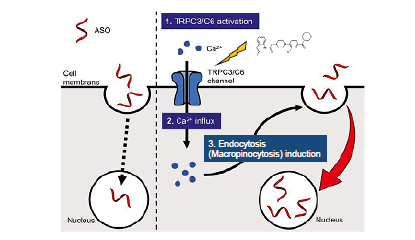
我々は、TRPC3/C6チャネルを選択的に活性化し、細胞内へのCa2+ 流入を促進する新規化合物 L687の取得に成功しました。L687とともに ASO を肺がん細胞に添加し、ASO の細胞内移行性と遺伝子発現抑制活性を評価したところ、細胞内の ASO 量は L687の濃度および培養時間依存的に増加し、それに伴って標的遺伝子の発現量が減少しました。Ca2+ キレート剤、TRPC 阻害剤、TRPC3/C6 siRNA による処理、また、マクロピノサイトシス阻害剤(飲作用阻害剤)の処理を行ったところ、ASO の細胞内取り込みが顕著に抑制されました。
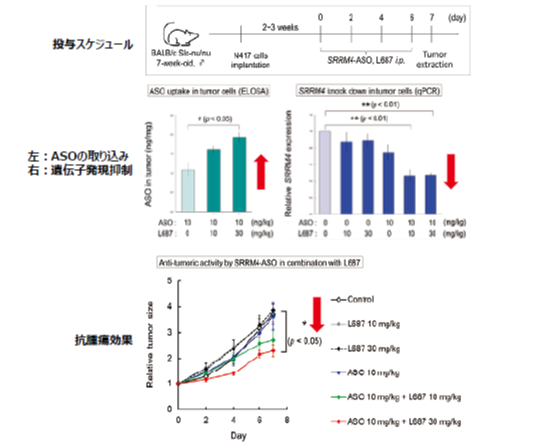
これらの結果から、L687による ASO の細胞内取り込み亢進にはTRPC3/C6チャネルを介した Ca2+ 流入と、続くマクロピノサイトシスの誘導が関与している可能性が高いことがわかりました。動物実験でも小細胞肺がん由来の細胞を背部に移植した担癌マウスに腫瘍の増殖に関わる遺伝子を標的とする ASO (SRRM4 ASO)と L687を腹腔内投与したところ、ASO 単独投与群に比べ、併用投与群では有意な腫瘍組織への ASO の移行量の増加、SRRM4遺伝子発現の減少、腫瘍サイズ増大の抑制効果が確認できました。
研究の意義と将来展望
本研究の結果から、TRPC3/C6チャネルを発現するがんに対し、増殖にかかわる遺伝子を標的とする ASO と L687を併用投与する手法は新たながん疾患治療となることが期待できます。ASO の細胞内取り込みを増強して DDS として機能する低分子はいまだ知られておらず、本研究が新たな DDS 開発の重要な一歩となることを期待します。

担当研究者
教授 小比賀 聡 (薬学研究科 生物有機化学分野)、准教授 下條 正仁(薬学研究科 生物有機化学分野)、特任准教授 永田 龍 (薬学研究科 生物有機化学分野)
キーワード
核酸医薬/アンチセンス核酸/TRPC3/C6チャネル/活性化剤/DDS
応用分野
医療・ヘルスケア、創薬
参考URL
https://www.phs.osaka-u.ac.jp/homepage/b007/
https://researchmap.jp/read0014368
https://researchmap.jp/shimojom
https://researchmap.jp/0292
