研究 (Research)
最終更新日:
発酵食品に含まれる免疫活性化因子、酢酸菌リピドAの化学合成と機能評価 (Immune activating factor from fermented foods: Chemical synthesis and function of acetic acid bacterial lipid A)
准教授 下山 敦史 (理学研究科 化学専攻)、特任教授(常勤) 深瀬 浩一(放射線科学基盤機構) SHIMOYAMA Atsushi (Graduate School of Science), FUKASE Koichi (Institute for Radiation Sciences)
研究の概要
グラム陰性菌の細胞外膜成分である糖脂質リピド A は代表的な自然免疫活性化因子として知られており、我々は近年、低炎症性リピド Aをアジュバントとして開発してきた。
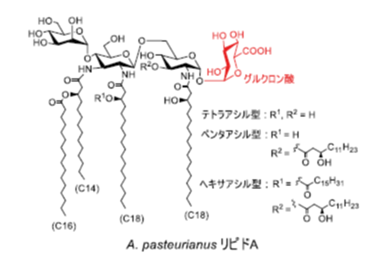
本研究では、宿主免疫機能の向上、アレルギー症状の改善などが経験的に報告されている発酵黒酢に着目し、その製造に使用されている酢酸菌Acetobacter pasteurianus 由来リピド A を、食経験から経口投与の安全性が担保された安全で安定なアジュバント候補物質として期待し、マンノースおよびグルクロン酸を含むユニークな四糖骨格からなるA. pasteurianus リピド A を挑戦的な立体選択的1,1′- α , α – グリコシル化を含む合成戦略により世界で初めて合成した。
構造活性相関研究も展開し、A. pasteurianus リピド A に特徴的なグルクロン酸部位が免疫機能と耐酸性に重要であることも明らかにした。
研究の背景と結果
グラム陰性菌の細胞外膜成分リポ多糖(LPS)は代表的な活性化因子の一つであり、その活性中心は糖脂質リピド A である。代表的な大腸菌リピド A は、強力な免疫賦活作用を有する一方で致死毒性を示し、アジュバントへの展開は困難である。我々のグループではこれまでに、腸管粘膜免疫制御組織であるパイエル板に共生しているAlcaligenes faecalis 由来のリピド A が、毒性を惹起せずに粘膜免疫と全身性免疫の双方を効果的に活性化できることを見い出し、有望な粘膜ワクチンアジュバントとして開発している。
一方で、A. faecalis リピドは、酸に不安定なグリコシルリン酸構造を有するため、経口投与した場合、胃酸中で分解してしまうことが想定される。酵素耐性なども必要になるが、まずはリピド A の耐酸性向上を目指した。食経験による安全性が期待でき、経口摂取による免疫活性化が示唆されていた発酵黒酢に含まれる酢酸菌A. pasteurianus リピド A に着目し、系統的合成によりA. pasteurianus LPS の活性中心構造の同定とリピド A の機能評価を実施した。
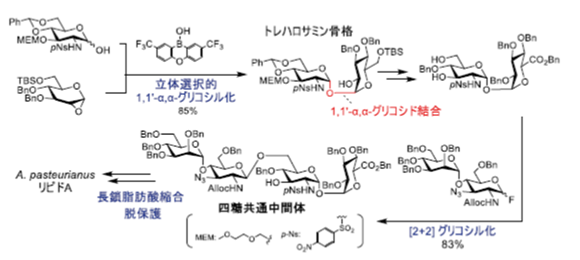
選択的構築が困難な1,1’- α , α – グリコシド結合を含むトレハロサミン骨格を、竹本らのトレハロース骨格構築(Angew. Chem. Int. Ed. 2020)を参考に、ボリン酸を触媒に用いたグリコシル化で効率的に構築した。糖受容体アミノ基保護基を検討し、p-Ns 体を用いることで高収率かつ高立体選択的に1,1’- α , α – グリコシドを得た。続いて、フッ化糖との [2+2] グリコシル化により四糖共通中間体を得た。長鎖脂肪酸導入、脱保護をへて、A. pasteurianus リピド A の初の合成を達成した。ヘキサアシル型が最も高い免疫賦活活性を示し、A. pasteurianusLPS の活性中心構造を同定した。さらには構造活性相関研究を展開し、グルクロン酸部位が免疫機能と耐酸性に重要であることも明らかにし、耐酸性リピド A デザインの指針を示した。
研究の意義と将来展望
アジュバントとは、ワクチンの効果を高めるために、ワクチンと共に投与される物質である。抗原のみでは効果的に免疫を獲得できないため、ワクチンの効力を高めるためにアジュバントの添加が必要であるが、有効性と安全性を兼ね備えたアジュバント開発は簡単ではない。酢酸菌リピド A は、安全性、化学安定性と免疫活性化作用を併せ持つアジュバントのシーズとして期待される。
担当研究者
准教授 下山 敦史 (理学研究科 化学専攻)、特任教授(常勤) 深瀬 浩一(放射線科学基盤機構)
キーワード
アジュバント/ワクチン/酢酸菌/免疫/グリコシル化
応用分野
医療・ヘルスケア、ワクチン
参考URL
https://www.chem.sci.osaka-u.ac.jp/lab/fukase/
https://researchmap.jp/ashimo_
https://researchmap.jp/read0076573
