研究 (Research)
最終更新日:
老化と肥満に共通するオートファジー停滞に着目した腎臓病進展の病態解明 (Stagnation of autophagy as a driver of kidney disease progression in aging and obesity)
特任助教(常勤) 山本 毅士、教授 猪阪 善隆 (医学系研究科 腎臓内科学) YAMAMOTO Takeshi, ISAKA Yoshitaka (Graduate School of Medicine)
研究の概要
慢性腎臓病(CKD)は、20歳以上の約5人に1人が罹患し、新たな国民病とされています。加齢や肥満は CKD 発症や進行に深く関与しますが、本研究ではそれに対抗する新たな機構を解明しました。これまで私たちは加齢や肥満に伴う腎臓病において、腎尿細管のオートファジーが保護的に働く一方で、腎臓病が進行するとリソソーム負担のためオートファジーがこれ以上活性化できなくなる「オートファジー停滞」が生じることを示してきました。しかし、オートファジー停滞が生じた際に腎臓の健康を維持する代償機構は不明でした。
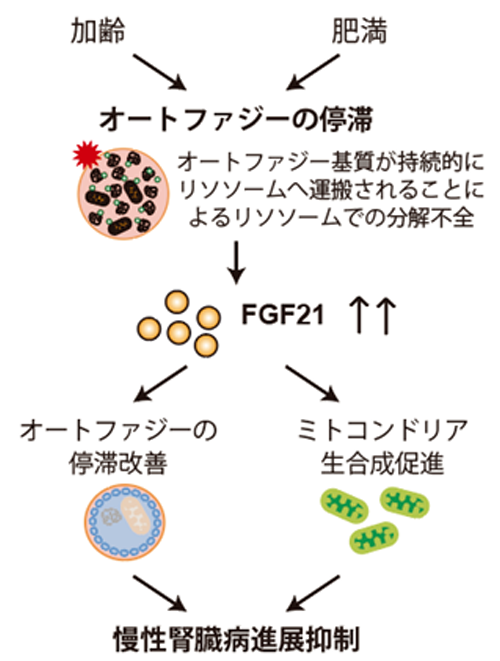
本研究により、加齢や肥満時に尿細管でオートファジーが活性化されないことが、抗老化・抗肥満因子として知られる FGF21の産生を誘導することが明らかになりました。さらに、産生された FGF21がオートファジー停滞を改善し、ミトコンドリアの生合成を促進することで、CKD 進展を抑制することが示されました。
研究の背景と結果
CKD は、20歳以上の約5人に1人が罹患する新たな国民病とされ(CKD 診療ガイド2024)、その発症や進行には加齢や肥満が深く関与しています。オートファジーは、細胞質成分の品質管理やエネルギー状態の最適化を通じて細胞の恒常性を維持しています。近年、私たちは腎尿細管細胞におけるオートファジーが加齢や肥満による腎臓病に対抗する役割を果たす一方で、加齢や肥満に伴い腎尿細管細胞がリソソームストレスによってオートファジーをこれ以上活性化できなくなる「オートファジー停滞」状態に陥ることを明らかにしました。しかし、このオートファジー停滞に対抗する機構は未解明のままでした。
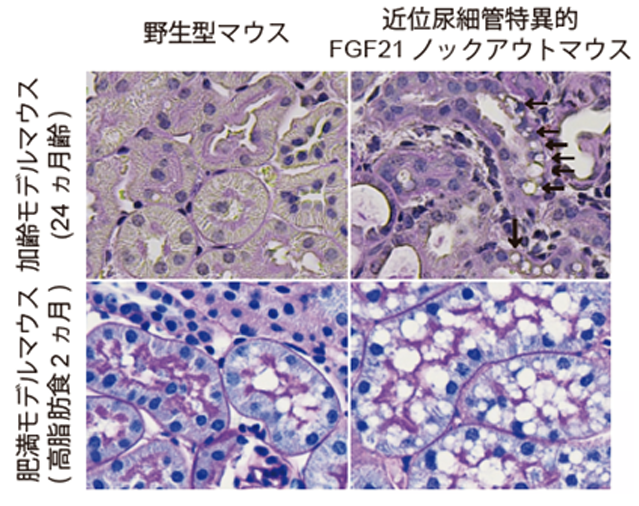
そこで、オートファジーに必要な遺伝子である Atg5を近位尿細管特異的に欠損させたオートファジー不全マウスを作製し、加齢モデル(24ヶ月飼育)および肥満モデル(高脂肪食負荷2ヶ月間)を用いて腎臓における FGF21の産生を検証しました。その結果、いずれのモデルにおいてもオートファジー不全マウスで FGF21産生が顕著に増加していることが確認されました。さらに、近位尿細管特異的 FGF21ノックアウト(KO)マウスを作製し、加齢および肥満モデルで検証したところ、FGF21 KO マウスでは尿細管内に巨大リソソームを伴う空胞変性が顕著に増加し(図2)、オートファジー停滞も悪化していることが示されました。
加えて、オートファジー不全マウスおよびオートファジー不全かつFGF21 KO マウスを作製し、加齢および肥満モデルで検証したところ、オートファジー不全かつ FGF21 KO マウスはオートファジー不全マウスと比較して腎臓病の進展が顕著であることが明らかになりました。さらに、このマウスではミトコンドリア生合成の低下やミトコンドリアの異常も確認されました。これらの結果から、近位尿細管においてオートファジー不全時に産生される FGF21が、オートファジー停滞の改善やミトコンドリア生合成の促進を通じて腎保護的に機能することが示されました。
研究の意義と将来展望
本研究は、FGF21やオートファジー停滞を標的とした新しい CKD治療の確立に道を開くものです。オートファジーの仕組みを解明し、2016年にノーベル生理学・医学賞を受賞した大隅良典博士の業績から8年が経ちました。近い将来、オートファジー研究が腎疾患治療に応用され、透析を必要とする腎不全の抑制が実現する日が来ると確信しています。
担当研究者
特任助教(常勤) 山本 毅士、教授 猪阪 善隆 (医学系研究科 腎臓内科学)
キーワード
慢性腎臓病/加齢/肥満/FGF21/オートファジー
応用分野
医療・ヘルスケア、創薬
参考URL
https://www.med.osaka-u.ac.jp/pub/kid/kid/index.html
https://researchmap.jp/tyamamoto-handai3857
https://researchmap.jp/isaka-handai3857
